3/19/2026
Amidbindungen sind allgegenwärtige, wichtige Struktureinheiten in Peptidwirkstoffen, niedermolekularen Wirkstoffen und Funktionsmaterialien. Wir haben bereits mehrere Studien zu Amidierungsreaktionen von Aminen und Carbonsäuren vorgestellt und damit vielfältige Syntheseansätze für die Säure-Amin-Kondensation aufgezeigt. Heute widmen wir uns einem neuen Ansatz. Das Team um Batra, S., berichtete über eine neuartige Amidsynthesemethode, die die einstufige, direkte Reaktion von Nitro- (oder Nitroso-) Verbindungen mit Aryl -α -Ketocarbonsäuren zur Herstellung von Amiden ermöglicht.
Amidbindungen sind allgegenwärtige, wichtige Struktureinheiten in Peptidwirkstoffen, niedermolekularen Wirkstoffen und Funktionsmaterialien. Wir haben bereits mehrere Studien zu Amidierungsreaktionen von Aminen und Carbonsäuren vorgestellt und damit vielfältige Syntheseansätze für die Säure-Amin-Kondensation aufgezeigt. Heute widmen wir uns einem neuen Ansatz. Das Team um Batra, S., berichtete über eine neuartige Amidsynthesemethode, die die einstufige, direkte Reaktion von Nitro- (oder Nitroso-) Verbindungen mit Aryl -α -Ketocarbonsäuren zur Herstellung von Amiden ermöglicht.
Das Besondere an dieser Forschung ist die Demonstration einer innovativen, einstufigen Methode zur direkten Synthese von Amiden in wässrigem Medium, die ohne Übergangsmetalle und Reduktionsmittel auskommt. Die Methode ist einfach durchzuführen und arbeitet unter milden Bedingungen. Sie eignet sich für ein breites Spektrum an Substraten, ist umweltfreundlich und bietet eine neue Möglichkeit zur grünen Synthese von Amidverbindungen.
I. Traditioneller Ansatz
Bei herkömmlichen Methoden zur Synthese von Amiden aus Nitroverbindungen muss typischerweise zunächst die Nitrogruppe zu einer Aminogruppe reduziert werden, gefolgt von einer Amidierungsreaktion mit einer aktivierten Carbonsäure oder in Gegenwart eines Kondensationsmittels. Dieses Verfahren ist nicht nur umständlich, sondern auch anfällig für die Bildung von Nebenprodukten.
Das Team um Batra, S. verfolgte einen anderen Ansatz und nutzte geschickt einen Radikalmechanismus, um die direkte Amidierung von Nitro- (oder Nitroso-) Verbindungen zu erreichen. Kern ihrer Methode ist die Verwendung von Kaliumpersulfat in einer alkalischen wässrigen Lösung zur Erzeugung von Sulfatradikalen. Diese abstrahieren dann Wasserstoffatome von Aryl -α-Ketocarbonsäuren, decarboxylieren diese und erzeugen so das entscheidende Benzoylradikal , wodurch die Amidbindung geknüpft wird .
II. Optimale Reaktionsbedingungen und Substratuniversalität
In der Studie von Batra, S. und seinem Team erforderten die Reaktionsbedingungen ein wässriges System, und sowohl Initiator als auch Base mussten Kaliumsalze sein. Die optimalen Reaktionsbedingungen waren: Acetonitril /Wasser (1:1) als Lösungsmittel, Kaliumcarbonat (1,5 Äquivalente) als Base , Kaliumpersulfat (3,0 Äquivalente) als Initiator sowie Nitro- (bzw. Nitroso-)Verbindungen (1,0 Äquivalente) und Aryl -α-ketocarbonsäuren (2,1 Äquivalente), die bei 80 °C zu den entsprechenden Amiden reagierten . Die Studie zeigte außerdem, dass der Erfolg der Reaktion stark von der Verwendung von Kaliumsalzen abhing .
Dieses Verfahren weist eine gute Substratverträglichkeit auf und eignet sich für die folgenden Substrattypen.
(1) 3-Nitroisoxazol-Substrate: Unabhängig davon, ob der aromatische Ring eine elektronenspendende Gruppe (z. B. Methyl) oder eine elektronenziehende Gruppe (z. B. Cyano) trägt, verläuft die Reaktion problemlos und liefert das entsprechende Amidprodukt in exzellenter Ausbeute. Auch verschiedene substituierte Aryl -α- Ketocarbonsäuren können an der Reaktion teilnehmen.
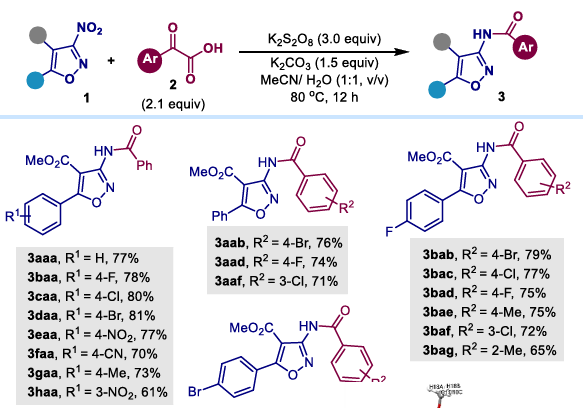
Allerdings benötigen Isoxazol-Substrate eine elektronenziehende Gruppe an der 4-Position, damit die Umwandlung erfolgen kann; eine Amidierung ist ohne Substitution nicht möglich.
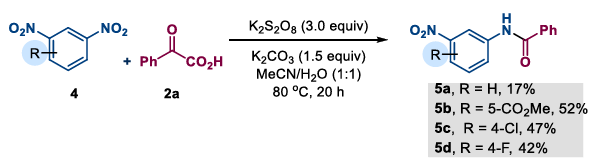
(2) 1,3-Dinitrobenzol-Substrate: Das Team untersuchte auch Amidierungsreaktionen von 1,3-Dinitrobenzol und seinen Derivaten und erhielt die entsprechenden N-(3-Nitrophenyl)benzamid-Produkte in Ausbeuten von 17–52 %. Diese Methode bietet einen neuen Weg zur direkten Derivatisierung von Polynitroverbindungen.
(3) Nitrosylsubstrate: Aufgrund eines tiefen Verständnisses des Mechanismus haben Forscher diese Strategie erfolgreich auf Nitrosylverbindungen übertragen. Unter denselben Bedingungen liefern Nitrosylverbindungen und Aryl -α- ketocarbonsäuren direkt eine Reihe strukturell vielfältiger Amide in mittleren bis hohen Ausbeuten. Diese Transformation ist auf eine Vielzahl substituierter Nitrosylaromaten, heterocyclischer Nitrosylverbindungen und aliphatischer Nitrosylverbindungen anwendbar.
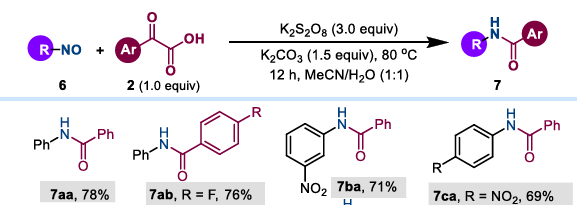
Noch interessanter ist die Erkenntnis der Studie, dass N-Benzoylphenylhydroxylamin in wässriger Lösung in Gegenwart von Kaliumpersulfat direkt in Amide umgewandelt werden kann, ohne dass eine Base benötigt wird. Mit anderen Worten: Solange die Struktur des Reaktionssubstrats eine bestimmte Stufe des Reaktionsmechanismus erfüllt, können Amide mit dieser Methode synthetisiert werden.
III. Reaktionsmechanismus: Radikalgetriebene Amidreaktion
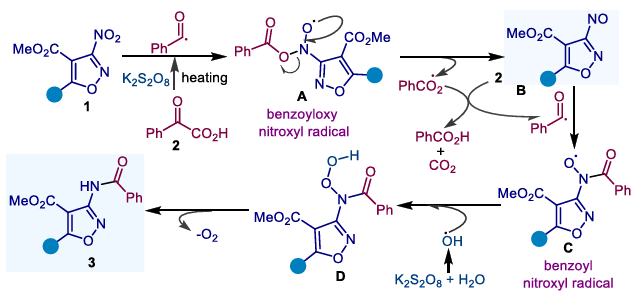
Das Team schlug folgenden Reaktionsmechanismus vor: Am Beispiel von 3-Nitroisoxazol-Substraten zersetzt sich Kaliumpersulfat in alkalischem Milieu bei hohen Temperaturen und bildet Sulfatradikale. Diese abstrahieren Wasserstoffatome von Aryl -α-Ketocarbonsäuren und unterliegen einer Decarboxylierung, wodurch Benzoylradikale entstehen. Diese Radikale greifen anschließend die Nitrogruppe im nitroaromatischen Kohlenwasserstoff an und abstrahieren ein Sauerstoffatom, wodurch Benzoyloxyradikale und nitrosoaromatische Kohlenwasserstoff-Zwischenprodukte gebildet werden. Das Benzoyloxyradikal reagiert mit einem weiteren Molekül Aryl- α-Ketocarbonsäure und regeneriert so Benzoylradikale. Ein zweites Benzoylradikal verbindet sich mit einem nitrosoaromatischen Kohlenwasserstoff zu einem Benzoylnitrosoradikal-Zwischenprodukt. Schließlich verbindet sich dieses Radikal mit im System gebildeten Hydroxylradikalen und unterliegt einer Desoxygenierung, wodurch letztendlich das Zielamidprodukt entsteht.
IV. Synthese, Anwendung und Zusammenfassung
Zusammenfassend entwickelte diese Studie eine direkte Amidierungsmethode, die mild, einfach durchzuführen, umweltfreundlich und ohne Übergangsmetalle oder Reduktionsmittel ist. Durch einen radikalischen Transformationsprozess gelang die effiziente und umweltfreundliche Umwandlung von 3-Nitroisoxazolen, 1,3-Dinitrobenzolen und Nitrosoverbindungen in Amide. Dies eröffnet einen attraktiven neuen Syntheseweg für verwandte Amidverbindungen und liefert wichtige theoretische Grundlagen sowie praktische Beispiele für die grüne Synthesechemie .
Unternehmensvorstellung:
Suzhou Haofan Biotech Co., Ltd. (Börsenkürzel: 301393.SZ), gegründet 2003 und mit Hauptsitz in der Suzhou High-Tech-Zone, ist ein nationales Hightech-Unternehmen, das pharmazeutische Forschungs- und Entwicklungs- sowie Produktionsunternehmen weltweit mit Spezialrohstoffen beliefert. Die Produkte werden hauptsächlich in der Synthese von Peptiden, Nukleotiden und Arzneimitteln eingesetzt und umfassen ein breites Spektrum, darunter Kondensationsmittel für spezielle Amidbindungen, Schutzmittel, Vernetzungsmittel, Proteinvernetzungsmittel für Antikörper-Wirkstoff-Konjugate, molekulare Bausteine, Liposomen und Phosphorreagenzien. Bis heute hat das Unternehmen über 1.500 verschiedene Produkte entwickelt und hergestellt.
Nach über zwei Jahrzehnten kontinuierlicher Anstrengungen und stetiger Weiterentwicklung hat Haofan Biotech seine Expertise im Bereich globaler Peptidsynthese-Reagenzien kontinuierlich ausgebaut. Das Unternehmen hat sich zu einem führenden Anbieter mit einem breiten Spektrum an kundenspezifischen Produkten und bedeutenden Vorteilen in der Großproduktion entwickelt und ist in der Lage, die spezifischen Bedürfnisse verschiedenster Kunden zu erfüllen. Wir laden alle Interessenten herzlich ein, sich mit uns in Verbindung zu setzen, um mehr über unser Produkt zu erfahren und Kooperationsmöglichkeiten auszuloten .
Referenzen:
[1] Dekarboxylativ/OxidativAmidierungvonArylα‐KetocarbonsäureSäuren mit Nitroarenen und Nitrosoverbindungen in wässrigem Medium.
DOI: 10.1021/acs.orglett.0c03666
Hier stellen wir Ihnen unsere beliebten verwandten Produkte vor, die Sie interessieren könnten. Wenn Sie Fragen haben, setzen Sie sich bitte mit uns in Verbindung; unsere Spezialisten werden Ihnen innerhalb von 24 Stunden antworten.
Bitte füllen Sie das untenstehende Formular aus und unser Vertriebsteam wird Ihnen gerne ein Angebot für Peptidsynthesereagenzien unterbreiten.