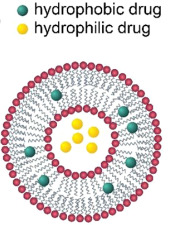
Liposomen sind die Vorstufe von Lipid-Nanopartikeln. Es handelt sich um kleine geschlossene Vesikel, die spontan aus einer Phospholipid-Doppelschicht gebildet werden. Sie ähneln im Aufbau Zellmembranen und können die Eigenschaften von Zellmembranen nachahmen. Liposome wurden von Bangham et al. entdeckt. in den 1960er Jahren entwickelt und dienten zunächst als einfaches Modell zur Untersuchung der Struktur und Funktion von Zellmembranen. Mit der Weiterentwicklung der Technologie und eingehenderer Forschung haben sich Liposomen nach und nach zu einem potenziellen Träger für die Arzneimittelabgabe entwickelt. Aufgrund ihrer amphipathischen Struktur können Liposomen verschiedene Wirkstoffe transportieren. Hydrophile Arzneimittel können im wässrigen Innenbereich von Liposomen eingeschlossen werden, während hydrophobe Arzneimittel im Kohlenwasserstoffkettenbereich der Lipiddoppelschicht eingekapselt werden können, wie unten gezeigt.
Liposomenzusammensetzung
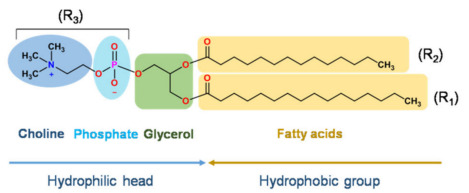
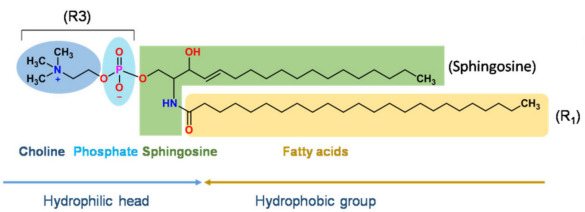
Zur Arzneimittelabgabe verwendete Liposome bestehen hauptsächlich aus verschiedenen Arten von Phospholipiden und Cholesterin, deren Grundgerüst Phospholipide (Glycerophospholipide und Sphingomyelin) bilden. Glycerophospholipide sind Lipide mit Glycerin als Rückgrat, und Sphingomyelin ist ein Lipid mit Sphingosin als Rückgrat. Die folgende Abbildung zeigt die Grundstrukturen von Glycerophospholipiden und Sphingomyelin.
Schematische Darstellung der Struktur von Glycerophospholipiden
Schematische Darstellung der Struktur von Sphingomyelin
Hinweis: R1 und R2 können gesättigte oder ungesättigte Fettsäuren wie Laurinsäure, Palmitinsäure, Ölsäure, Erucasäure usw. sein. R3 kann neutrales Phosphatidylcholin (PC), Phosphatidylethanolamin (PE) oder geladenes Phosphatidylserin (PS) sein ), Phosphatidylinositol (PI) oder Phosphatidsäure bei verschiedenen pH-Werten. (PA), Phosphatidylglycerol (PG)
Cholesterin ist ein amphipathisches neutrales Lipid, das die Fließfähigkeit der Lipiddoppelschicht regulieren, die Liposomenstabilität erhöhen, den Arzneimittelaustritt reduzieren und eine Rolle bei der Verlängerung und Kontrolle der Arzneimittelfreisetzung spielen kann.
Zusätzlich zu Phospholipiden und Cholesterin können Liposomen auch Membranmaterialien wie Polysaccharide (wie Oligosaccharide, Chitosan und Hyaluronsäure) und Tenside zugesetzt werden, um die Stabilität der Liposomen zu verbessern und die Arzneimittelfreisetzung zu regulieren.
Liposomenklassifizierung
Je nach Struktur und Eigenschaften können Liposomen in Typen wie unilamellare Liposomen, multilamellare Liposomen und multivesikuläre Liposomen unterteilt werden. Darüber hinaus können Liposomen je nach Ladung in kationische Liposomen (wie DOTAP), anionische Liposomen (wie DOPS) und neutrale Liposomen (wie DSPE) unterteilt werden. Je nach Funktion gibt es auch Liposomen mit langer Zirkulation, glykosylmodifizierte Liposomen, wärmeempfindliche Liposomen, pH-empfindliche Liposomen, Immunoliposomen, magnetische Liposomen, elastische Liposomen usw.
Vorteile und Stabilität von Liposomen
Liposomen sind thermisch instabile Systeme und anfällig für Probleme wie Arzneimittelaustritt und -abbau. Für eine zielgerichtete Therapie ist die Stabilität von Liposomen ein unverzichtbarer Faktor. Die Stabilität von Liposomen umfasst physikalische Stabilität, chemische Stabilität und biologische Stabilität. Unter physikalischer und chemischer Stabilität versteht man im Allgemeinen die Fähigkeit einer Liposomenformulierung, ihre Eigenschaften über einen bestimmten Zeitraum beizubehalten. Phospholipide unterliegen chemischen Abbaureaktionen wie der Hydrolyse von Esterbindungen und der Peroxidation ungesättigter Acylketten. Diese Phänomene können die Langzeitstabilität von Liposomenformulierungen beeinträchtigen. Um die Integrität der Liposomenvesikelstruktur aufrechtzuerhalten, ist es außerdem notwendig, die verschiedenen Wechselwirkungskräfte innerhalb und zwischen Liposomen auszugleichen. Die Wahl gesättigter Phospholipide oder Phospholipide mit niedriger Sättigung, eine geeignete Doppelschichtkonzentration, geeignete Puffertypen und die Zugabe von Antioxidantien, Metallchelatbildnern und Kryoschutzmitteln können die Stabilität von Liposomen erhöhen.
Unter biologischer Stabilität versteht man die Fähigkeit von Liposomen, ihre Integrität in Gegenwart von Serumproteinen aufrechtzuerhalten. Im Blut kommt es nach der Bindung von Liposomen an Serumproteine zu einer Opsonisierung, die zu einer schnellen Clearance der Liposomen führt. Um die biologische Stabilität zu erhöhen, können Substanzen wie Polyethylenglykol (PEG) zugesetzt werden, um eine Opsonisierung zu vermeiden und die Zirkulationszeit der Liposomen im Blut zu verlängern.
Liposomen ähneln in ihrer Struktur biologischen Membranen und weisen eine gute Biokompatibilität auf. Als Arzneimittelträger haben Liposomen die folgenden Vorteile:
1. Sie können verschiedene Arten von Arzneimitteln/Genen transportieren: Liposomen verfügen über eine spezielle Doppelschichtstruktur, die viele verschiedene Arten von Arzneimitteln und Genen, einschließlich wasserlöslicher und fettlöslicher Arzneimittel, versiegeln und schützen kann.
2. Potenzial für die Arzneimittelverabreichung auf verschiedenen Wegen: Liposomen können auf verschiedenen Wegen verabreicht werden, einschließlich oraler Verabreichung, Injektion, topischer Anwendung usw. Der am besten geeignete Verabreichungsweg kann je nach spezifischem Bedarf ausgewählt werden.
3. Verhindern Sie den chemischen und biologischen Abbau: Liposomen haben eine ähnliche Struktur wie Zellmembranen und können Arzneimittel vor chemischem und biologischem Abbau schützen, die Halbwertszeit von Arzneimitteln verlängern und die Stabilität und Bioverfügbarkeit von Arzneimitteln verbessern.
4. Reduzieren Sie unspezifische Nebenwirkungen und Toxizität von Medikamenten: Liposomen können Medikamente im Inneren versiegeln, die Wirkung von Medikamenten auf Nichtzielgewebe reduzieren, unspezifische Nebenwirkungen und Toxizität reduzieren und die Wirksamkeit und therapeutischen Indikatoren von Medikamenten verbessern.
5. Vielseitige chemische Modifizierungs- und Targeting-Fähigkeiten: Liposomen können chemisch modifiziert werden, um Targeting-Effekte zu erzielen, indem spezifische Liganden oder funktionelle Gruppen angehängt werden, um das Wirkstoff-Targeting und die Selektivität zu verbessern.
6. Kompatibel mit biologisch abbaubaren und ungiftigen Materialien: Liposomen können mit biologisch abbaubaren und ungiftigen Materialien kompatibel sein, um schädliche Auswirkungen auf den menschlichen Körper zu reduzieren.
Liposomenanwendung
Da Liposome eine gute Biokompatibilität, Ungiftigkeit und vielfältige Wirkstofftransportfähigkeiten aufweisen, haben Liposomen breite Anwendungsaussichten in Arzneimittelabgabesystemen. Der Erfolg der Forschung von Doxil hat die Forschung und Entwicklung von Liposomen-Arzneimittelverabreichungssystemen inspiriert, sodass Liposomen in verschiedenen Bereichen der Krankheitsbehandlung weit verbreitet sind.
Die wichtigste Anwendung von Liposomen bei der Arzneimittelabgabe ist die Krebsbehandlung. Krebs, eine Krankheit, bei der sich gesunde Körperzellen unkontrolliert teilen, gilt als eine der größten medizinischen Herausforderungen dieses Jahrhunderts. Im Allgemeinen ist die Gefäßpermeabilität von Tumorstellen in der Regel höher und Liposome können über kapillare Epithelzellen gezielt in Tumorgewebe gelangen. Darüber hinaus ist die Liposomenstruktur äußerst flexibel und kann mit verschiedenen Polymeren und Formulierungen modifiziert werden. Körper usw., um die Stabilität zu verbessern und zielgerichtetere Effekte zu erzielen. Liposome sind in der Lage, Arzneimittel mit unterschiedlichen physikalisch-chemischen Eigenschaften zu transportieren und gelten daher als ideal für die Arzneimittelabgabe und Krebsbehandlung in der Nanomedizin. Im Bereich der Krebsbehandlung haben Liposomen-Arzneimittelverabreichungssysteme großes Potenzial gezeigt. Im Laufe der Jahre haben sich mit der Vertiefung der Forschung die therapeutischen Ansätze und Methoden von Liposomen als Antitumor-Wirkstoffträger immer weiter verbreitet. Derzeit werden einige Medikamente zur Krebsbehandlung eingesetzt, beispielsweise Marqibo® (Vincristin), Lipusu (Paclitaxel) und Onivyde® (Irinotecan) usw.
Ein weiterer wichtiger Anwendungsbereich ist die antimykotische Behandlung. Pilzinfektionen stellen eine zunehmende Bedrohung für die menschliche Gesundheit dar, insbesondere für immungeschwächte Bevölkerungsgruppen, wobei invasive Pilzinfektionen eine besonders hohe Morbidität und Mortalität verursachen. Als natürliche Barriere für Pilze beeinträchtigt Biofilm die Wirkung von Antimykotika auf Bakterien, verringert die Arzneimittelaufnahme und erschwert die Wirksamkeit von Antimykotika. Als Wirkstoffträger weisen Liposome eine gute Biokompatibilität auf und können die toxischen Wirkungen und Nebenwirkungen von Arzneimitteln reduzieren. Eine Struktur, die einer biologischen Membran ähnelt, kann mit der Plasmamembran der mikrobiellen Zelle verschmelzen und hohe Konzentrationen von Arzneimitteln in die Zellmembran oder das Zytoplasma freisetzen, wodurch eine effizientere Abgabe erreicht und ein Arzneimittelausfluss vermieden wird. Zu den Arzneimitteln, die derzeit zur antimykotischen Behandlung eingesetzt werden, gehören Amphotericin-B-Liposomen wie Ambisome®, Abelcet® und Amphotec®.
Neben der Krebsbehandlung und der antimykotischen Behandlung finden Liposomen auch in anderen Bereichen vielfältige Anwendungsmöglichkeiten. Beispielsweise werden bei der Behandlung von Augenkrankheiten Liposomen-Arzneimittelabgabesysteme zur Behandlung von Augeninfektionen eingesetzt. Darüber hinaus können Liposomen auch zur Malariabehandlung, zur Herstellung von Liposomenimpfstoffen (z. B. Grippeimpfstoffen) und zur Überwindung biologischer Barrieren (z. B. Blut-Hirn-Schranke, Behandlung der Alzheimer-Krankheit) eingesetzt werden und haben gute Ergebnisse erzielt.
Allerdings war die Produktion von Liposomen in großem Maßstab eine Herausforderung und kostspielig, was zu einer hohen Marktposition von Liposomen führte. Dennoch bestehen angesichts der Fortschritte in Wissenschaft und Technologie weiterhin hohe Erwartungen an die weitere Entwicklung von Liposomen und Nanomedizin als Arzneimittelabgabesysteme.
Referenzen:
[1] Pattni, BS; Chupin, VV; Torchilin VP Neue Entwicklungen in der liposomalen Arzneimittelabgabe[J]. Chem. Rev. 2015, 115, 10938-10966.
[2] Yang Fuyu. Liposom in der Biofilmforschung und pharmakologischen Anwendungen[J]. Fortschritte in Biochemie und Biophysik. 1977, 06, 36-40.
[3] Tenchov, R.; Vogel, R.; Zhou, QQ; et al. Lipid-Nanopartikel – von Liposomen bis zur mRNA-Impfstoffabgabe, eine Landschaft der Forschungsvielfalt und des Fortschritts[J]. ACS Nano. 2021, 15, 16982-17015.
[4] Liu, P.; Chen, GL; Zhang, JC Ein Überblick über Liposomen als Arzneimittelabgabesystem: Aktueller Status zugelassener Produkte, regulatorisches Umfeld und Zukunftsperspektiven[J]. Moleküle. 2022, 27, 1372-1394. [5]
Liu Yang, Lu Wanliang, Zhang Qiang. Liposomen- und Nanopartikel-Arzneimittelabgabesysteme Forschungsfortschritt von [J]. Zeitschrift der Chinesischen Akademie der Medizinischen Wissenschaften. 2006, 28, 583-589.
[6] Hussain, A.; Singh, S.; Sharma, D.; et al. Elastische Liposomen als neuartige Träger: jüngste Fortschritte bei der Arzneimittelabgabe[J]. Int J Nanomedizin. 2017, 12, 5087-5108.
[7] Torchilin, VP Jüngste Fortschritte bei Liposomen als pharmazeutische Träger[J]. Nat Rev Drug Discov. 2005, 4, 145–160.
[8 ] Filipczak, N.; Pan, JY; Yalamarty, SSK; et al. Jüngste Fortschritte in der Liposomentechnologie[J]. Erweiterte Bewertungen zur Arzneimittelabgabe. 2020, 156, 4-22.
[9] Groß, DE; Abdelmessih, RG; Fink, EA; et al. Liposomenzusammensetzung beim Design, der Synthese, der Charakterisierung und der klinischen Anwendung der Arzneimittelabgabe[J]. Erweiterte Bewertungen zur Arzneimittelabgabe. 2021, 176, 113851 [
10] Huang Ziyuan, Sun Yuqi, Hu Haiyang, Zhuang Rui, Xu Qi, Chen Dawei. Forschungstechniken und -methoden zur Stabilität von Liposomenformulierungen[J]. Acta Pharmaceutical Sinica, 2016, 51, 356-361.
[11] Samad, A.; Sultana, Y.; Aqil, M. Liposomale Arzneimittelabgabesysteme: Eine aktuelle Übersicht[J]. Aktuelle Medikamentenlieferung. 2007, 4, 297-305.
[12] Ebrahim, S.; Peyman, GA; Lee, PJ Anwendungen von Liposomen in der Augenheilkunde[J]. Surv Ophthalmol. 2005, 50, 167-182.
[13] Nsairat, H.; Khater, D.; Sayed, U.; et al. Liposomen: Struktur, Zusammensetzung, Typen und klinische Anwendungen[J]. Heliyon. 2022, 8, 9394.
[14] Rommasi, F.; Esfandiari, N. Liposomale Nanomedizin: Anwendungen für die Arzneimittelabgabe in der Krebstherapie[J]. Nanoscale Res Lett. 2021, 16, 95.
[15] Chen Shuisheng, Zhou Keqian, Li Xiaodong, Lu Quanzhen, Yu Yuan. Anwendung und Mechanismus von Nano-Arzneimittelverabreichungssystemen bei der Behandlung antimykotischer Infektionen. Acta Pharmaceutical Sinica, 2021, 56, 1893-1901.