3/13/2026
Amidbindungen sind nicht nur die grundlegende Struktureinheit von Peptidmolekülen, sondern auch die zentrale Struktureinheit vieler Naturstoffe und Wirkstoffe. Mit der zunehmenden Komplexität des Designs bioaktiver Moleküle haben sich die aufwendigen Schutzgruppen- und Abspaltungsschritte traditioneller Peptidsynthesestrategien zu einem Engpass entwickelt, der die Syntheseeffizienz einschränkt, die Syntheseroute verlängert und potenziell Nebenreaktionen sowie geringere Ausbeuten verursacht.
I. Hintergrund und Einleitung:
Amidbindungen sind nicht nur die grundlegende Struktureinheit von Peptidmolekülen, sondern auch die zentrale Struktureinheit vieler Naturstoffe und Wirkstoffe. Mit der zunehmenden Komplexität des Designs bioaktiver Moleküle haben sich die aufwendigen Schutzgruppen- und Abspaltungsschritte traditioneller Peptidsynthesestrategien zu einem Engpass entwickelt, der die Syntheseeffizienz einschränkt, die Syntheseroute verlängert und potenziell Nebenreaktionen sowie geringere Ausbeuten verursacht.
Die direkte Kondensation ungeschützter Aminosäuren hat sich in den letzten Jahren zu einem wichtigen Forschungsschwerpunkt entwickelt. Ziel dieser Methode ist es, den Syntheseprozess zu vereinfachen, Kosten zu senken und die Atomökonomie zu verbessern. Aufbauend auf ihren früheren Arbeiten zur silanvermittelten direkten Kondensation von Aminosäuren konzentriert sich das Team um Yamamoto, H. nun auf metallorganische Reagenzien – Trimethylaluminium (Me₃Al ) –, um deren Anwendung in der Peptidsynthese zu erforschen.
II. Trimethylaluminium:
Trimethylaluminium ist eine hochreaktive Lewis-Säure mit starker Elektrophilie und Methylierungskapazität. Als Organoaluminium-Reagenz kann es an verschiedenen Reaktionen teilnehmen und bietet dabei einzigartige Vorteile, insbesondere bei der Aktivierung von Carboxylgruppen und der Förderung von Amidierungsreaktionen. Da Trimethylaluminium jedoch mit Wasser reagiert, ist es mitunter gefährlich und erfordert daher besondere Fachkenntnisse im Umgang.
Vor den Forschungen von Yamamoto, H.s Team zur Trimethylaluminium-vermittelten Peptidsynthese gab es bereits mehrere Studien zur Verwendung von Trimethylaluminium für die Amidsynthese.
III. Frühe Erkundung:
1. Das Forschungsteam von Pfizer berichtete bereits über die Verwendung von Trimethylaluminium zur Förderung der direkten Kondensation von ungeschützten Carbonsäuren und Aminverbindungen. Der Wirkmechanismus besteht in der Bildung von Aluminat-Zwischenprodukten zur Knüpfung von Amidbindungen .
In der Substrateignungsstudie wurde 4-Phenylbenzoesäure als fixierte Carbonsäure verwendet und Amidierungsreaktionen mit verschiedenen Aminverbindungen durchgeführt. Unter Einwirkung von Trimethylaluminium wurden primäre, sekundäre und aromatische Amine in exzellenten Ausbeuten zu den Zielamiden erhalten.
Des Weiteren wurden unter Verwendung von 4-Phenylbenzylamin als fixer Aminkomponente Reaktionen mit verschiedenen Carbonsäuren durchgeführt. Dabei zeigte sich, dass aromatische Säuren im Allgemeinen eine bessere Aktivität aufwiesen als Fettsäuren.
2. Martin und sein Team entwickelten eine Methode zur Förderung der Reaktion von Aminosäureestern mit freien Aminosäuren unter Verwendung von Trimethylaluminium zur Bildung von Peptidbindungen. Diese Methode nutzt Carbonsäureester oder N-geschützte Aminosäureester als Elektrophile zur direkten Kupplung mit freien Aminosäuren oder Dipeptiden und erzielt dabei gute Ausbeuten. Bei dem Versuch, die Peptidkette zur Synthese von Tri- und Tetrapeptiden zu verlängern, tritt jedoch eine signifikante Racemisierung auf, was die Anwendung der Methode in der Synthese langer Peptide einschränkt.
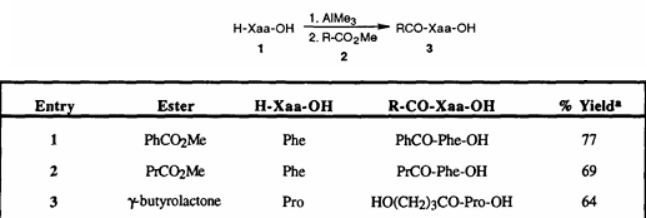
Während die oben genannten Studien das Potenzial und den Anwendungswert von Trimethylaluminium bei der Amidierung bestätigt haben, weisen sie im Allgemeinen Einschränkungen bei der Synthese langer Peptidketten auf und können den Anforderungen der Herstellung komplexer Peptidstrukturen nicht gerecht werden.
IV. Eintopf-Peptidsynthesestrategie :
Das Team um Yamamoto, H., entwickelte eine Eintopf-Peptidsynthesestrategie basierend auf einem Fünfringmechanismus. Diese Methode nutzt die Multifunktionalität von Trimethylaluminium voll aus, welches sowohl die Carboxylgruppe aktiviert als auch den nukleophilen Angriff der Aminogruppe koordiniert, wodurch eine effiziente und hoch stereoselektive Peptidsynthese ermöglicht wird.
1. Eintopf-Reaktionsmechanismus
Der Wirkungsmechanismus ist wie folgt: Zuerst reagiert Trimethylaluminium mit freien Aminosäuren, um die Carboxylgruppe zu aktivieren und Methan freizusetzen; dann reagiert es mit einer intramolekularen Aminogruppe, um ein fünfgliedriges Ringzwischenprodukt A zu bilden und ein zweites Molekül Methan freizusetzen; dann greift unter der Katalyse eines weiteren Moleküls Trimethylaluminium der neu hinzugefügte Aminosäureester das Zwischenprodukt A an, um eine Ringöffnungsreaktion einzugehen, wodurch das Zwischenprodukt B entsteht; schließlich wird durch Säurebehandlung die Aminogruppe freigesetzt, wodurch das Dipeptidprodukt entsteht.
Sollte es notwendig sein, die Peptidkette weiter zu verlängern, kann der obige Zyklus auf der Grundlage der Synthese von Dipeptiden wiederholt werden, oder es kann Fmoc-geschütztes Aminoacylchlorid zur Endkappenbildung im letzten Schritt eingeführt werden, wodurch die Peptidkettenlänge präzise kontrolliert wird.
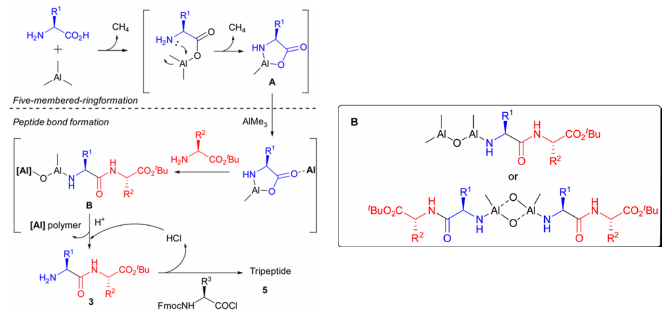
2. Optimierung der Reaktionsbedingungen
Das Team nutzte die Tripeptidsynthese als Modellreaktion, um die Reaktionsbedingungen zu untersuchen. Schließlich wurde Dichlormethan als Lösungsmittel verwendet und freie Aminosäuren sowie Trimethylaluminium bei niedriger Temperatur (0 °C ) vorgemischt, um die Carboxylgruppe zu aktivieren. Anschließend wurde das Tripeptid bei Raumtemperatur mit Aminosäuremethylester amidiert und mit Pentylsäure behandelt, um die vollständige Freisetzung der Aminogruppe zu gewährleisten. Abschließend wurde das Tripeptid durch Umsetzung mit Fmoc zum Schutz des Aminoacylchlorids erhalten.
3. Ausgezeichnete Kompatibilität mit funktionellen Gruppen und Stereoselektivität
Diese Synthesestrategie zeichnet sich durch eine ausgezeichnete Funktionalgruppenverträglichkeit aus, ist tolerant gegenüber Aminosäuren mit Seitenketten sowie Aminosäuren mit Estergruppen, Etherbindungen und schwefelhaltigen Gruppen und liefert eine hohe Reaktionsausbeute. Während des gesamten Syntheseprozesses wurde keine nennenswerte Racemisierung beobachtet, und die Stereoselektivität ist gut.
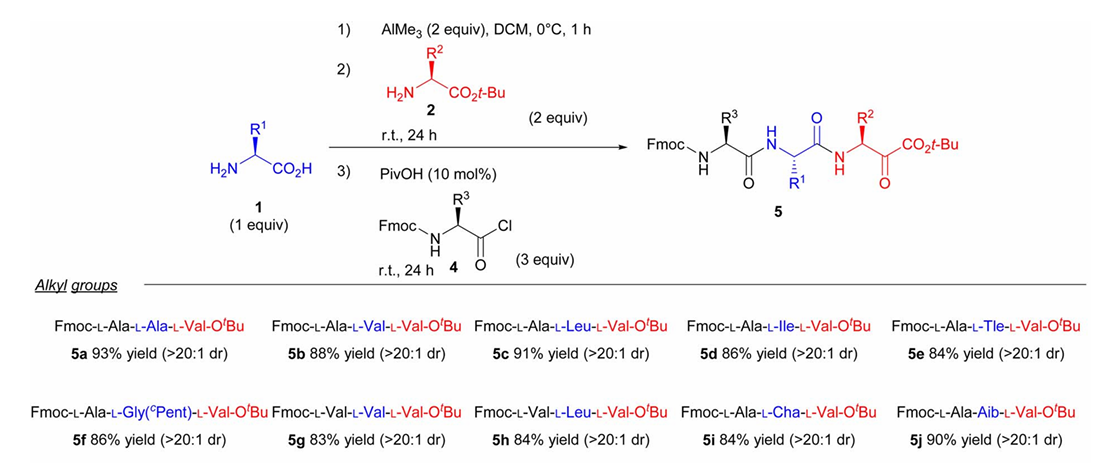
Aufbauend auf diesen Erkenntnissen untersuchte das Team die schrittweise Synthese von Tetra- und Pentapeptiden und erzielte dabei eine Ausbeute von rund 60 %, was eine gute Skalierbarkeit belegt. Bemerkenswert ist, dass die Studie ergab, dass die Kettenlänge und die Ausbeute der synthetisierten Peptide maßgeblich von der Produktlöslichkeit beeinflusst werden.
V. Gesamtschlussfolgerung:
Zusammenfassend lässt sich sagen, dass Trimethylaluminium ein kostengünstiges, leicht verfügbares, effizientes und racemarmes Kondensationsreagenz ist. Durch seine Verwendung entfällt die Voraktivierung der Carbonsäure, wodurch die Anzahl der Syntheseschritte und der Reagenzienverbrauch deutlich reduziert werden. Es zeigt zudem eine gute Kompatibilität mit funktionellen Gruppen und ermöglicht die einfache Herstellung von Zielpeptiden unter milden Bedingungen. Dieser Durchbruch eröffnet einen neuartigen Ansatz für die Synthese von Peptidwirkstoffen und funktionellen Peptidmaterialien.
Unternehmensvorstellung:
Suzhou Haofan Biotech Co., Ltd. (Börsenkürzel: 301393.SZ), gegründet 2003 und mit Hauptsitz in der Suzhou High-Tech-Zone, ist ein nationales Hightech-Unternehmen, das pharmazeutische Forschungs- und Entwicklungs- sowie Produktionsunternehmen weltweit mit Spezialrohstoffen beliefert. Die Produkte werden hauptsächlich in der Synthese von Peptiden, Nukleotiden und Arzneimitteln eingesetzt und umfassen ein breites Spektrum, darunter Kondensationsmittel für spezielle Amidbindungen, Schutzmittel, Vernetzungsmittel, Proteinvernetzungsmittel für Antikörper-Wirkstoff-Konjugate, molekulare Bausteine, Liposomen und Phosphorreagenzien. Bis heute hat das Unternehmen über 1.500 verschiedene Produkte entwickelt und hergestellt.
Nach über zwei Jahrzehnten kontinuierlicher Anstrengungen und stetiger Weiterentwicklung hat Haofan Biotech seine Expertise im Bereich globaler Peptidsynthese-Reagenzien kontinuierlich ausgebaut. Das Unternehmen hat sich zu einem führenden Anbieter mit einem breiten Spektrum an kundenspezifischen Produkten und bedeutenden Vorteilen in der Großproduktion entwickelt und ist in der Lage, die spezifischen Bedürfnisse verschiedenster Kunden zu erfüllen. Wir laden alle Interessenten herzlich ein, sich mit uns in Verbindung zu setzen, um mehr über unser Produkt zu erfahren und Kooperationsmöglichkeiten auszuloten .
Referenzen:
[1] Trimethylaluminium-vermittelte direkte Amidierung von Carbonsäuren.
DOI: 10.1055/s-0030-1260982
[2] Anwendung von AlMe3-vermittelten Amidierungsreaktionen zur Peptidsynthese in Lösung.
DOI: 10.1016/s0040-4039(98)00071-9
[3] Trimethylaluminium-vermittelte Eintopf-Peptidverlängerung .
DOI: 10.1039/d3sc00208j
Hier stellen wir Ihnen unsere beliebten verwandten Produkte vor, die Sie interessieren könnten. Wenn Sie Fragen haben, setzen Sie sich bitte mit uns in Verbindung; unsere Spezialisten werden Ihnen innerhalb von 24 Stunden antworten.
Bitte füllen Sie das untenstehende Formular aus und unser Vertriebsteam wird Ihnen gerne ein Angebot für Peptidsynthesereagenzien unterbreiten.