I. Hintergrund und Einleitung:
Diese effiziente, zyklische Synthesestrategie aus Schutzgruppen-Kondensation und -Abspaltung erhöht jedoch die Anzahl der Peptidsyntheseschritte, den Reagenzienverbrauch und den Arbeitsaufwand erheblich. Daher ist die Entwicklung einer Methode, die Aminosäure-Kreuzkondensationsreaktionen direkt und ohne Schutzgruppen ermöglicht, die beste Lösung.
Kürzlich schlug das Team um Yamamoto, H. einen hocheffizienten und umweltfreundlichen Syntheseweg auf Basis von Siliciumreagenzien vor: Aminosäuren werden mit Siliciumreagenzien modifiziert, um sie elektrophil und nukleophil zu machen, und anschließend ohne Verwendung traditioneller Schutzgruppen direkt kondensiert, um effizient Peptidbindungen zu knüpfen. Diese Methode vereinfacht nicht nur die Syntheseschritte, sondern zeichnet sich auch durch ihre hervorragende Praktikabilität aus.
II. Einführung in die Prinzipien:
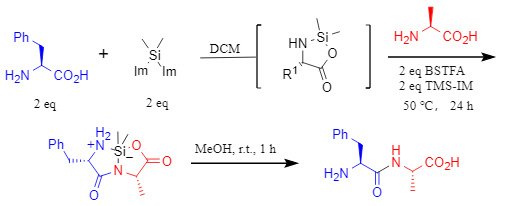
Kern dieser Studie ist der synergistische Effekt zweier Silanreagenzien zur hochselektiven Amidbindungsknüpfung zwischen ungeschützten Aminosäuren. Konkret reagiert ein Aminosäuremolekül mit Bis(1-imidazolyl)dimethylsilan in Dichlormethan zu einem elektrophilen, siliciumhaltigen, fünfgliedrigen cyclischen Zwischenprodukt, das als Acyl-Donor für Folgereaktionen mit anderen Nukleophilen zu den entsprechenden Produkten dient (siehe Abbildung 1). Ein anderes Aminosäuremolekül bildet unter der kombinierten Einwirkung von N-Trimethylsilylimidazolium (TMS-IM) und N,O-Bis(trimethylsilyl)trifluoracetamid (BSTFA) einen Aminosäure-TMS-Ester als Nukleophil.
Abbildung 1
In diesem System fungiert BSTFA primär als Silylierungsreagenz, während TMS-IM eine Doppelfunktion erfüllt: Zum einen reagiert es mit Aminosäuren und erhöht so deren Löslichkeit in Dichlormethan; zum anderen unterstützt es die Silylierung. Der synergistische Effekt dieser beiden Reagenzien verbessert die Selektivität der Reaktion signifikant und führt letztendlich durch elektrophile und nukleophile Reaktionen zu einem silan-cyclischen Dipeptid mit der korrekten Sequenz.
Darüber hinaus zeigt das resultierende silan-cyclische Dipeptid unter Normalbedingungen eine gute Stabilität und benötigt lediglich eine schnelle Behandlung mit Methanol bei Raumtemperatur, um das ungeschützte Dipeptid zu erhalten. Dies erleichtert die nachfolgende Verlängerung oder Reinigung (Abbildung 2).
Abbildung 2
III. Anwendungen:
1. Breites Substratspektrum und ausgezeichnete Stereoselektivität
Diese Synthesestrategie zeigt eine gute Kompatibilität mit Aminosäuren unterschiedlicher Strukturen (Abbildung 3). Ob es sich um eine Aminosäure mit sterisch anspruchsvoller Seitenkette oder ein Phenylalaninderivat mit verschiedenen elektronischen Eigenschaften handelt, das Zielprodukt kann in hoher Ausbeute (meist über 80 %) erhalten werden, wobei die Stereokonfiguration der Aminosäure gut erhalten bleibt (dr > 20:1). Selbst bei Phenylglycin (Phg), das zur Racemisierung neigt, bleibt die Stereokonfiguration erhalten, was die Überlegenheit dieser Methode hinsichtlich der Stereoselektivität beweist.
Abbildung 3
2. Effiziente Verlängerung von Dipeptid zu Polypeptid
Die mittels dieser Synthesestrategie erhaltenen silan-cyclischen Dipeptid-Zwischenprodukte sind stabil, leicht handhabbar und lassen sich problemlos in ungeschützte Dipeptide überführen. Gleichzeitig bieten sie eine einzigartige Plattform für die Peptidkettenverlängerung. Sowohl der N-Terminus als auch der C-Terminus können ohne den Einsatz herkömmlicher Kondensationsreagenzien direkt gekoppelt werden, wodurch die Bildung von Oxazolon und die damit verbundenen Epimerisierungsprobleme, die häufig bei der Synthese langer Peptidketten auftreten, effektiv vermieden werden.
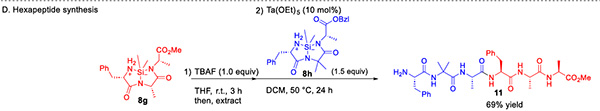
Diese Studie demonstriert zudem das Anwendungspotenzial dieser Strategie für den Aufbau komplexer Sequenzen. Durch die direkte Kondensation zwischen silan-cyclischen Tripeptiden wurden erfolgreich Hexapeptid- und Heptapeptidsequenzen synthetisiert (Abbildung 4). Das Heptapeptid-Grundgerüst findet sich in zahlreichen Wirkstoffmolekülen wie Smegglutid und Telposid. Diese „konvergente" Synthesestrategie, die Zielsequenzen durch direkte Verknüpfung von Peptidsegmenten aufbaut, vereinfacht den Syntheseprozess erheblich und bietet einen neuartigen Ansatz für die Herstellung komplexer Peptide und Peptidwirkstoffe.
Abbildung 4
IV. Gesamtschlussfolgerung:
Zusammenfassend entwickelte diese Studie eine Methode zur Bildung ungeschützter, chemisch selektiver Peptidbindungen zwischen Aminosäuren auf Basis von Siliciumreagenzien und erreichte die Synthese aggregierter Peptide. Diese Methode reduziert nicht nur die Anzahl der Syntheseschritte und den Reagenzienverbrauch signifikant, sondern bietet auch einen bequemen Weg zur Herstellung von Zielpeptiden unter milden Bedingungen. Dieser Durchbruch eröffnet einen neuen Syntheseweg für das Gebiet der Peptidsynthese und dürfte die Weiterentwicklung von Peptidwirkstoffen und verwandter Forschungsbereiche fördern.
Unternehmensvorstellung:
Suzhou Highfine Biotech Co., Ltd. (Börsenkürzel: 301393.SZ), gegründet 2003 und ansässig in der Suzhou High-Tech-Zone, ist ein nationales Hightech-Unternehmen, das Spezialrohstoffe für die pharmazeutische Forschung und Entwicklung sowie die Produktion weltweit anbietet. Die Produkte werden hauptsächlich in der Peptid-, Nukleotid- und pharmazeutischen Synthese eingesetzt und umfassen ein breites Spektrum, darunter Kondensationsmittel für die spezielle Amidbindungsknüpfung, Schutzmittel, Vernetzungsmittel, Proteinvernetzungsmittel für Antikörper-Wirkstoff-Konjugate, molekulare Bausteine, Liposomen und Phosphorreagenzien. Aktuell entwickelt und produziert das Unternehmen über 1500 Produkte.
Durch mehr als zwei Jahrzehnte kontinuierlicher Anstrengungen und stetiger Weiterentwicklung hat Highfine Biotech seine Expertise im Bereich globaler Peptidsynthese-Reagenzien kontinuierlich ausgebaut und sich zu einem führenden Unternehmen mit einem umfassenden Angebot an kundenspezifischen Produkten und bedeutenden Vorteilen in der Großproduktion entwickelt, das in der Lage ist, die spezifischen Bedürfnisse verschiedenster Kunden zu erfüllen. Wir laden interessierte Kunden herzlich ein, sich für weitere Informationen und zur Besprechung von Kooperationsmöglichkeiten mit uns in Verbindung zu setzen.
Referenzen:
[1] Peptidbindung zwischen ungeschützten Aminosäuren: Konvergente Synthese von Oligopeptiden. DOI: https://doi.org/10.1021/jacs.4c08049