3/26/2026
Als essenzielle Bestandteile von Lebensprozessen sind Peptide aufgrund des Bedarfs an effizienten und präzisen Synthesemethoden seit jeher ein Forschungsschwerpunkt der chemischen Synthese. Traditionelle Peptidsynthesemethoden beinhalten typischerweise die Aktivierung der Carboxylgruppe, wodurch diese in einen aktiven Ester oder eine andere reaktive Substanz umgewandelt wird, die dann mit einer Aminogruppe in einem anderen Molekül reagiert. Obwohl diese Methode weit verbreitet ist, beschränkt sie sich üblicherweise auf die C→N-Synthese und neigt bei empfindlichen Aminosäuren wie Cystein zu Nebenreaktionen wie der Racemisierung. Um diesen Engpass zu überwinden, hat das Team um J.-M. Campagne einen anderen Ansatz gewählt und eine neuartige Peptidsynthesemethode entwickelt, die auf einer „umgekehrten Aktivierungsstrategie“ basiert – also der Aktivierung der Aminogruppe.
Als essenzielle Bestandteile von Lebensprozessen sind Peptide aufgrund des Bedarfs an effizienten und präzisen Synthesemethoden seit jeher ein Forschungsschwerpunkt der chemischen Synthese. Traditionelle Peptidsynthesemethoden beinhalten typischerweise die Aktivierung der Carboxylgruppe, wodurch diese in einen aktiven Ester oder eine andere reaktive Substanz umgewandelt wird, die dann mit einer Aminogruppe in einem anderen Molekül reagiert. Obwohl diese Methode weit verbreitet ist, beschränkt sie sich üblicherweise auf die C→N-Synthese und neigt bei empfindlichen Aminosäuren wie Cystein zu Nebenreaktionen wie der Racemisierung. Um diesen Engpass zu überwinden, hat das Team um J.-M. Campagne einen anderen Ansatz gewählt und eine neuartige Peptidsynthesemethode entwickelt, die auf einer „umgekehrten Aktivierungsstrategie" basiert – also der Aktivierung der Aminogruppe.
I. Umgekehrtes Denken von „Aktivierten Carbonsäuren" zu „Aktivierten Aminosäuren"
Der Kern traditioneller Methoden liegt in der Aktivierung der Carboxylgruppe. Das Team um Campagne, J.-M., verlagerte die Aktivierungsstelle jedoch geschickt auf die Aminogruppe. Sie verwendeten kostengünstiges und leicht verfügbares N,N'-Carbonyldiimidazol (CDI) in Gegenwart von Triethylamin zur Reaktion mit α -Aminosäureestern. Dabei entstand ein stabiles N-Imidazolium-Carboxyl-Aminosäureester-Zwischenprodukt, das isoliert werden konnte (Abbildung 1). Dieses Zwischenprodukt entspricht einer „aktivierten Aminogruppe" und ist über mehrere Monate stabil lagerfähig.
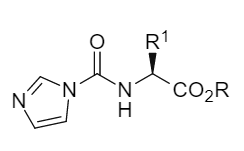
Abbildung 1 Allgemeine Formel des N-Imidazolylaminosäureesters
In der nachfolgenden Peptidsynthese reagiert dieses Zwischenprodukt direkt mit N-geschützten Aminosäuren in Dichlormethan unter milden, alkalifreien Bedingungen und in Gegenwart von Additiven (HOBt/CuBr₂ ) , wodurch Dipeptide in 52–90 % Ausbeute erhalten werden. Diese Methode ist mit gängigen Carbamat-Schutzgruppen wie Fmoc, Boc und Cbz kompatibel, und es wurde keine Racemisierung beobachtet, wenn das Reaktionssubstrat leicht racemisches Cystein enthielt. Studien zeigen jedoch, dass das herkömmliche Lösungsmittel für die Peptidsynthese, DMF, für dieses System ungeeignet ist.
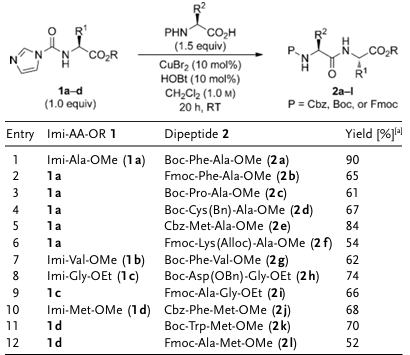
Abbildung 2. Synthese von Dipeptiden über „aktivierte Aminogruppen"
Um das Potenzial dieser Synthesestrategie weiter zu bestätigen, versuchte das Team, ein Tetrapeptid in N→C-Richtung zu synthetisieren und erhielt schließlich das Zielprodukt in 25% Ausbeute, ohne racemische Produkte zu finden. Diese Entdeckung demonstriert das erhebliche Potenzial dieser Methode für die reverse Peptidsynthese und bietet einen zuverlässigen neuen Weg zur Synthese komplexer Peptidwirkstoffe und bioaktiver Moleküle.
II. Eintopfsynthese: hohe Effizienz, Atomökonomie und gute Stereoselektivität.
Aufbauend auf früheren Arbeiten optimierte das Team um Campagne, J.-M. die Synthesestrategie und entwickelte eine Eintopf-Methode zur Synthese von Dipeptiden. Diese Methode, die ebenfalls unter milden, neutralen Bedingungen durchgeführt wird, benötigt keine zusätzliche Lauge und erzeugt N-Imidazolium-Carboxyl-Aminosäureester-Zwischenprodukte in situ. Ohne die Notwendigkeit einer Trennung und Reinigung können diese Zwischenprodukte direkt mit kommerziell erhältlichen geschützten Aminosäuren reagieren, was den Arbeitsprozess deutlich vereinfacht.
Experimentelle Ergebnisse zeigen, dass die Eintopf-Methode auch eine Vielzahl von Dipeptidderivaten effizient synthetisieren kann, mit Ausbeuten von bis zu 87 %. Sie ist mit verschiedenen N-Carbamat-Schutzgruppen kompatibel und weist eine ausgezeichnete stereochemische Stabilität auf. Weiterhin ergab die Studie, dass Prolin aufgrund seiner sekundären Aminstruktur nur schwer durch Aminoaktivierung zu Dipeptiden synthetisiert werden kann.
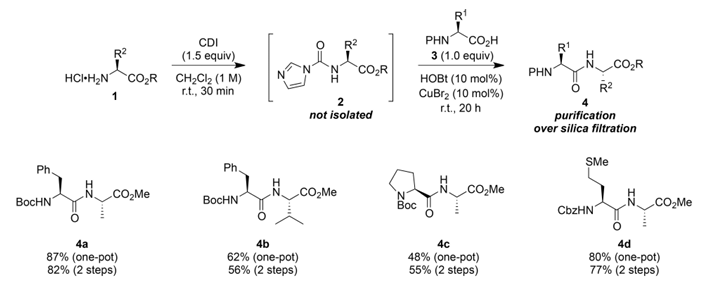
Abbildung 3 Eintopfsynthese von Dipeptiden
Im Gegensatz zum zweistufigen Verfahren nutzt die Eintopf-Strategie das im System entstehende Imidazol als Base während der „Aktivierung der Aminogruppe", wodurch ein Imidazolsalz gebildet wird und somit die Zugabe einer zusätzlichen Base entfällt. Die Studie ergab außerdem, dass die Zugabe einer zusätzlichen Base während der Kupplungsreaktion die Amidbindungsreaktion zwischen der aktivierten Aminogruppe und der Carbonsäure tatsächlich behindert.
III. Mikrowellenunterstützte Reaktion: beschleunigt die Reaktion und verkürzt die Zykluszeit
Zur Verbesserung der Syntheseeffizienz führte das Team von Campagne, J.-M. außerdem die mikrowellenunterstützte Technologie ein, um deren Anwendung in der "Amino-Aktivierungs"-Strategie zu erforschen.
Basierend auf der zweistufigen Synthese wurde Mikrowellenbestrahlung eingesetzt, um die Bindungsreaktion von Amiden zu fördern (Abbildung 4). Die Ergebnisse zeigten, dass Mikrowellen die Reaktionsgeschwindigkeit deutlich beschleunigen und die Reaktionszeit von 20 h (konventionelle Methode) auf 1 h verkürzen konnten, bei gleichzeitig guter Ausbeute und ohne Racemisierung. Darüber hinaus wurde die Methode auf die Synthese konventioneller Amide ausgeweitet, wobei die Ausbeute den Erwartungen entsprach.
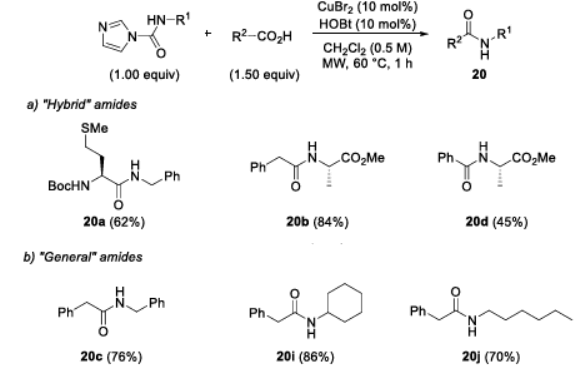
Abbildung 4 Mikrowellenunterstützte Synthese von Peptiden
Auf Grundlage experimenteller Beobachtungen schlug das Team einen möglichen plausiblen Reaktionsweg vor (Abbildung 5): Während der Reaktion wird ein gemischtes Carbamidanhydrid -Zwischenprodukt gebildet , gefolgt von einer intramolekularen Umlagerung und der Freisetzung von Kohlendioxid, wodurch schließlich die Zielpeptidbindung entsteht.
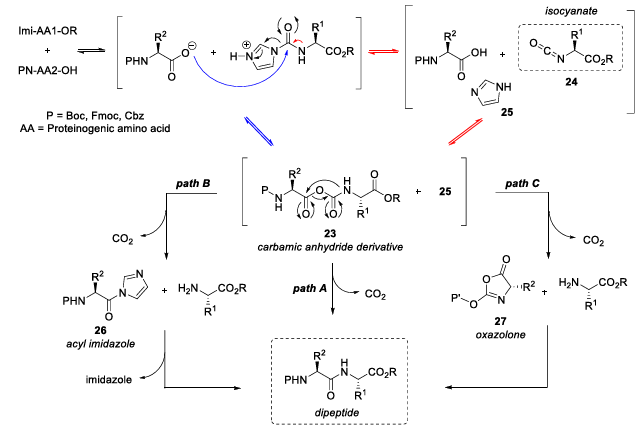
Abbildung 5 Reaktionsmechanismus
Zusammenfassend bietet die von Campagne, J.-M. und seinem Team entwickelte CDI-vermittelte α- Aminosäureester-Aktivierungsstrategie eine milde, praktische und atomökonomische neue Option zur Peptidbindungsknüpfung. Diese Methode vermeidet nicht nur effektiv die Racemisierung empfindlicher Aminosäuren während der Reaktion, sondern ermöglicht auch die anspruchsvolle Peptidsynthese in N→C-Richtung. Angesichts des stetig wachsenden Interesses an der Entwicklung von Peptidwirkstoffen dürfte diese innovative Synthesestrategie eine wichtige Ergänzung des Werkzeugkastens von Forschern darstellen.
Unternehmensvorstellung:
Suzhou Haofan Biotech Co., Ltd. (Börsenkürzel: 301393.SZ), gegründet 2003 und mit Hauptsitz in der Suzhou High-Tech-Zone, ist ein nationales Hightech-Unternehmen, das pharmazeutische Forschungs- und Entwicklungs- sowie Produktionsunternehmen weltweit mit Spezialrohstoffen beliefert. Die Produkte werden hauptsächlich in der Synthese von Peptiden, Nukleotiden und Arzneimitteln eingesetzt und umfassen ein breites Spektrum, darunter Kondensationsmittel für spezielle Amidbindungen, Schutzmittel, Vernetzungsmittel, Proteinvernetzungsmittel für Antikörper-Wirkstoff-Konjugate, molekulare Bausteine, Liposomen und Phosphorreagenzien. Bis heute hat das Unternehmen über 1.500 verschiedene Produkte entwickelt und hergestellt.
Nach über zwei Jahrzehnten kontinuierlicher Anstrengungen und stetiger Weiterentwicklung hat Haofan Biotech seine Expertise im Bereich globaler Peptidsynthese-Reagenzien kontinuierlich ausgebaut. Das Unternehmen hat sich zu einem führenden Anbieter mit einem breiten Spektrum an kundenspezifischen Produkten und bedeutenden Vorteilen in der Großproduktion entwickelt und ist in der Lage, die spezifischen Bedürfnisse verschiedenster Kunden zu erfüllen. Wir laden alle Interessenten herzlich ein, sich mit uns in Verbindung zu setzen, um mehr über unser Produkt zu erfahren und Kooperationsmöglichkeiten auszuloten .
Referenzen:
[1] Inverse Peptidsynthese über aktivierte α-Aminoester.
DOI: 10.1002/anie.201402147
[2] SequentiellEintopfSynthesevonDipeptidedurchDieVorübergehende BildungvonCDI-N-geschütztα-Aminoester .
DOI: 10.1002/adsc.201700034
[3] Aminaktivierung: „Inverse" Dipeptidsynthese und Amidfunktionsbildung durch aktivierte Aminoverbindungen .
DOI: 10.1021/acs.joc.2c01288
Hier stellen wir Ihnen unsere beliebten verwandten Produkte vor, die Sie interessieren könnten. Wenn Sie Fragen haben, setzen Sie sich bitte mit uns in Verbindung; unsere Spezialisten werden Ihnen innerhalb von 24 Stunden antworten.
Bitte füllen Sie das untenstehende Formular aus und unser Vertriebsteam wird Ihnen gerne ein Angebot für Peptidsynthesereagenzien unterbreiten.