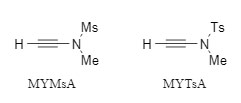1. Inamid (Zhao-Reagenz)
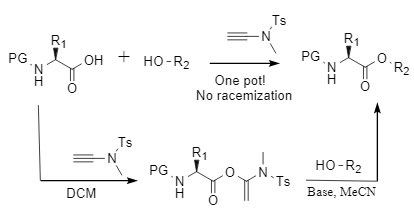
Alkinamid-Kondensationsreagenzien sind eine von Professor Zhao Junfeng entwickelte, nicht-racemisierende Kondensationsreagenziengruppe, die unter dem Namen Zhao-Reagenzien bekannt ist (siehe Abbildung 1). Die Kondensationsreaktion, an der sie beteiligt sind, erfordert keine zusätzlichen Katalysatoren und ist gut luft- und wasserbeständig. Das Zielamid wird unter nahezu neutralen Bedingungen erhalten, wodurch das durch Alkali verursachte Racemisierungsproblem vermieden wird. Zhao-Reagenzien wurden erfolgreich zum Aufbau aktiver Moleküle wie Amiden, Makroliden und Thioamiden durch die „Zwei-Schritt-Eintopf"-Synthesestrategie eingesetzt (Abbildung 2). Weitere Informationen finden Sie unter „Ein neuartiges, hocheffizientes, nicht-racemisierendes Alkinamid-Kondensationsreagenz".
Abbildung 1 Zhao-Reagenz
Abbildung 2 Kondensationsreaktion vermittelt durch Zhao-Reagenz
2. Allenon
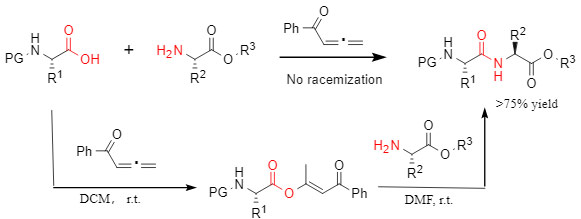
Die Forschungsgruppe von Professor Zhao Junfeng hat eine ketonvermittelte Amidbindungsmethode entwickelt, die eine neue Lösung für den Aufbau von Amidbindungen bietet. Diese Methode benötigt keine zusätzlichen Katalysatoren oder Additive. Der Reaktionsverlauf besteht darin, durch die Reaktion von Carbonsäure und Keton ein Ester-Intermediat zu erzeugen, das anschließend mit Amin zum entsprechenden Amidprodukt reagiert. Dadurch wird das Risiko einer Racemisierung vermieden und das Auftreten weiterer Nebenreaktionen reduziert. Gleichzeitig ist die Methode vielseitig an eine Vielzahl natürlicher und nicht-natürlicher Aminosäuren anpassbar. (Abbildung 3)
Abbildung 3 Phenylallenon-vermittelte Kondensationsreaktion
3. Oxyma-Serie
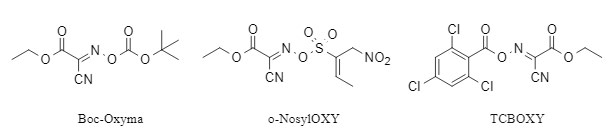
Da sich Oxyma bei Kondensationsreaktionen als bahnbrechender Vorteil gegenüber herkömmlichen Benzotriazol-Reagenzien erwies, erregte es rasch breite Aufmerksamkeit in der Wissenschaft. Es wurde eine Reihe von Oxyma-Derivaten entwickelt, die sich durch hohe Effizienz, Racemisierungsfreiheit und Explosionsgefahr auszeichnen. Die folgende Abbildung zeigt mehrere repräsentative Derivate der Oxyma-Reihe, die nicht racemisieren (siehe Abbildung 4). Die Oxyma-Nebenprodukte der Reaktion können recycelt und zu entsprechenden Derivaten regeneriert werden, wodurch die Menge an chemischen Abfällen minimiert wird. Derivate der Oxyma-Reihe werden bereits erfolgreich zum Aufbau wichtiger Struktureinheiten wie Amiden und Estern eingesetzt. Eine ausführliche Einführung finden Sie unter „Boc-Oxyma: Ein Wirkstoff, zwei Effekte für ein neues grünes Synthesesystem".
Abbildung 4 Oxyma-Derivate
4. TCFH-NMI
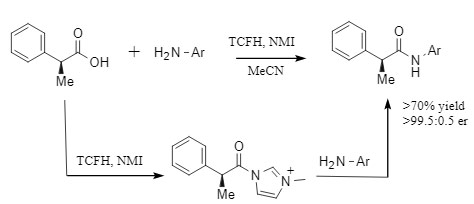
Die Kombination aus N,N,N',N'-Tetramethylchlorformamidinhexafluorophosphat (TCFH) und N-Methylimidazol (NMI) ist ein hocheffizientes Amidkondensationssystem, das von Bristol-Myers Squibb entwickelt wurde. Diese ideale Kombination fördert die Kondensationsreaktion durch die In-situ-Erzeugung hochreaktiver N-Acylimidazoliumsalze (siehe Abbildung 5). Sie bietet technische Vorteile wie eine breite Palette anwendbarer Substrate und die Vermeidung von Diastereoisomerisierung und eignet sich besonders für Kondensationsreaktionen mit schwach aktiven Aminen und großen sterisch gehinderten Carbonsäuren. Weitere Informationen finden Sie unter „Die ideale Kombination für effiziente Säure-Amin-Kondensation: TCFH-NMI".
Abbildung 5 TCFH-NMI-vermittelte Kondensationsreaktion
5. Xiangshan-Reagenz
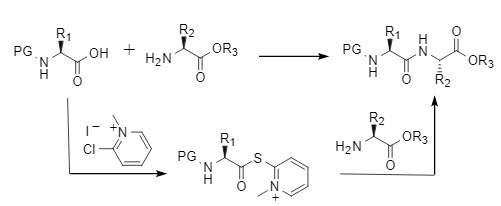
2-Chlor-1-methylpyridiniumiodid, kurz CMPI, ist auch als Mukaiyama-Reagenz bekannt. Es ist leicht zu handhaben und einfach nachzubearbeiten. Es ist ein Kondensationsreagenz mit kommerziellem Wert. Die Kondensationsreaktion mit CMPI erfolgt üblicherweise unter schwach alkalischen Bedingungen. Es aktiviert Carbonsäuren zu Carbonsäureestern und durchläuft anschließend durch nukleophilen Angriff Aminolyse- und Alkoholysereaktionen. Dadurch werden wichtige Struktureinheiten effizient aufgebaut und bieten hervorragende Kompatibilität mit funktionellen Gruppen sowie Racemisierungsinhibition (Abbildung 6).
Abbildung 6 Kondensationsreaktion vermittelt durch Mukaiyama-Reagenz
6. NDTP
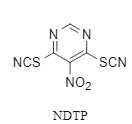
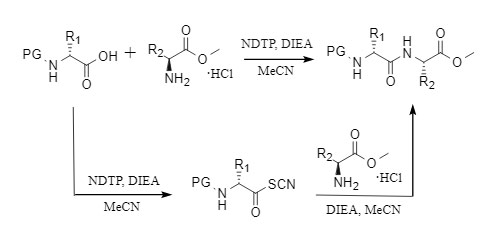
5-Nitro-4,6-dithiocyanatopyrimidin (NDTP, Abbildung 7), entwickelt von der Forschungsgruppe um Akademiker Wang Rui, ist ein neues Kondensationsreagenz, das mild, leicht verfügbar und recycelbar ist. NDTP fördert die Bildung von Carbonsäuren zu Acylthiocyanat-Zwischenprodukten mit hoher Stabilität und säurechloridähnlicher Aktivität. Diese werden dann von Amin-/Alkohol-Reagenzien angegriffen, die schnell und ohne Racemisierung Bindungen bilden können (Abbildung 8). Bemerkenswert ist, dass in der NDTP-vermittelten Veresterungsreaktion Ester unter milden Bedingungen innerhalb einer Minute gebildet werden können.
Abbildung 7 NDTP-Struktur
Abbildung 8 NDTP-vermittelte Kondensationsreaktion
7. T3P
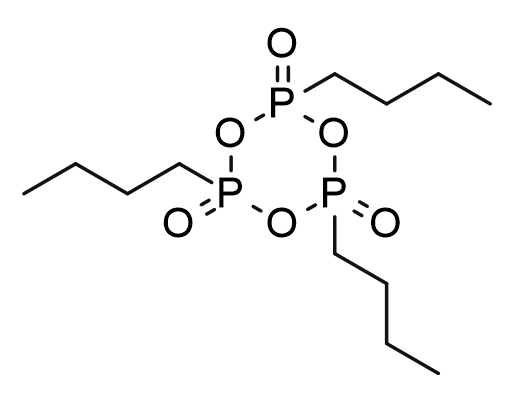
Eine milde Kombination aus n-Propylphosphonsäureanhydrid (T3P) und Pyridin wurde zum Aufbau von Amidbindungen entwickelt. Dieses System ermöglicht die Kupplungsreaktion einer Vielzahl leicht racemischer Substrate und liefert Amide in hohen Ausbeuten und hoher Enantiomerenreinheit. T3P ist derzeit als überwachte Chemikalie gelistet und unterliegt Einschränkungen hinsichtlich Transport, Verwendung, Lagerung usw. Alternativ bietet n-Butylphosphonsäureanhydrid (T4P) eine gleichwertige oder sogar höhere Reaktionseffizienz und Stereokontrolle (Abbildung 9).
Abbildung 9 Strukturformel von T3P und T4P
8. Andere Reagenzien
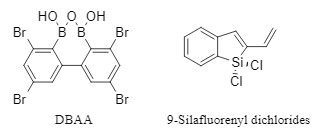
Zusätzlich zu den oben genannten Mainstream-Reagenzien werden nach und nach auch eine Reihe von Substanzen wie Silane und Borsäureanhydrid als Kondensationsreagenzien verwendet, die sich durch ihre hohe Aktivierungsfähigkeit, breite Substratanwendbarkeit und ausgezeichnete Racemisierungsinhibitionsfähigkeit auszeichnen.
![T3P- und T4P-Strukturen T3P- und T4P-Strukturen]()
Nach 22 Jahren unermüdlicher Anstrengungen und Akkumulation hat Haofan Biotech seine Präsenz auf dem Gebiet der globalen Reagenzien für die Peptidsynthese weiter ausgebaut und sich zu einem führenden Unternehmen mit umfassender Abdeckung kundenspezifischer Produkte und erheblichen Vorteilen bei der Massenproduktion entwickelt. Das Unternehmen ist nun in der Lage, Reagenzien zur Racemisierungsinhibition in unterschiedlichen Spezifikationen bereitzustellen, um die speziellen Bedürfnisse unterschiedlicher Kunden zu erfüllen. Kunden, die an diesem Produkt interessiert sind, laden wir herzlich ein, mit uns Kontakt aufzunehmen, um mehr über die Produktdetails zu erfahren und Kooperationsmöglichkeiten auszuloten.
Referenzen:
[1] Duengo, S.; Muhajir, M. I.; Maharani, R.; et al. Epimerisation in Peptide Synthesis[J]. Molecules, 2023, 28, 8017.
[2] Guo, Y. Y.; Wang, M. Y.; Gao, Y.; Liu, G. D. Recent advances in asymmetric synthesis of chiral amides and peptides: racemization-free coupling reagents[J]. Org. Biomol. Chem., 2024, 22, 4420-4435.
[3] Wang, X.W.; Yang, Y.; Zhao, J.F.; et al. Ynamide-Mediated Intermolecular Esterification[J]. J. Org. Chem. 2020, 85, 6188-6194.
[4] Wang, Z.N.; Wang, X.W.; Wang, P.H.; Zhao, J.F. Allenone-Mediated Racemization/Epimerization-Free Peptide Bond Formation and Its Application in Peptide Synthesis[J]. J. Am. Chem. Soc., 2021, 143, 10374-10381.
[5] Beutner, G.L.; Young, I.S.; Ye, Q.M.; et al. TCFH−NMI: Direct Access to N‑Acyl Imidazoliums for Challenging Amide Bond Formations[J]. Org. Lett. 2018, 20, 4218-4222.
[6] Li, Y.P.; Wang, P.; Wang, R.; et al. NDTP Mediated Direct Rapid Amide and Peptide Synthesis without Epimerization[J]. Org. Lett., 2022, 24, 1169-1174.