Unnatürliche Aminosäuren sind Aminosäuren, die in Tieren und Pflanzen nicht vorkommen, in der Natur selten sind oder künstlich synthetisiert werden. Sie sind Derivate natürlicher Aminosäuren und werden hauptsächlich in zwei Kategorien unterteilt. Eine Kategorie sind Aminosäureanaloga mit Strukturen, die denen natürlicher Aminosäuren ähneln, sich jedoch in der entgegengesetzten Konfiguration widerspiegeln, wie z. B. D-Alanin, D-Phenylalanin, D-Serin usw. Die andere Kategorie sind Aminosäureersatzstoffe mit Strukturen, die sich stark von natürlichen Aminosäuren unterscheiden. Unnatürliche
Aminosäuren haben verschiedene Seitenkettengruppen und stereochemische Eigenschaften. Mit der Entwicklung und Förderung von Wissenschaft und Technologie wurden sie in vielen Bereichen wie Medizin, Lebensmittel und chirale Synthese weit verbreitet eingesetzt. Die verschiedenen funktionellen Gruppen von UAAs, wie Carbonyl, Azid, Alkinyl, Alkenyl, Amid, Nitro, Phosphat und Sulfonat, ermöglichen es Proteinen, komplexere und vielfältigere Modifikationsreaktionen zu durchlaufen.
UAAs haben eine starke Spezifität und wenig Einfluss auf die ursprüngliche Struktur von Proteinen, was sie zu einem leistungsstarken Werkzeug zum Studium der Proteinstruktur und der dynamischen Konformation macht. So kann beispielsweise die Einführung fluorierter Aminosäuren an Schlüsselstellen von Proteinen die Signale von Proteinen in der Kernspinresonanz effektiv beobachten und so den Prozess der Datenerfassung und -analyse vereinfachen.
Darüber hinaus kann die Einführung unnatürlicher Aminosäuren die physikalischen und chemischen Eigenschaften von Proteinen verändern, wie etwa den pH-Wert und die Temperaturstabilität. In praktischen Anwendungen haben sich UAAs als wirksam erwiesen, um die Leistung von Enzymen zu verbessern, einschließlich der Steigerung der Enzymaktivität und -stabilität. So kann beispielsweise der Ersatz des 309. natürlichen Tyrosins der Phosphotriesterase durch L-(7-Hydroxycumarin-4-yl)ethylglycin oder L-(7-Methylcumarin-4-yl)ethylglycin die katalytische Aktivität des Enzyms für die Hydrolyse von Paraoxon auf der Grundlage seiner ursprünglich hohen Effizienz um das 8- bis 11-fache steigern. Darüber hinaus kann die Einfügung fluorierter Aminosäuren die thermische Stabilität von Enzymen deutlich verbessern. So kann beispielsweise Para-Fluorphenylalaninphosphatase auch bei einer hohen Temperatur von 60 °C noch ohne Beeinträchtigung normal funktionieren.
UAAs haben breite Anwendungsaussichten im Bereich der Biomedizin und sind auch die Hauptbestandteile synthetischer Peptide und peptidähnlicher Arzneimittel im In- und Ausland.
Seit der Entdeckung des Penicillins haben Antibiotika unzählige Leben gerettet und gelten als eine der wichtigsten medizinischen Errungenschaften des 20. Jahrhunderts. Der übermäßige Einsatz von Antibiotika in der menschlichen und tierischen Gesundheit hat jedoch zur Entstehung antibiotikaresistenter Bakterien geführt, insbesondere multiresistenter „Superbakterien", die eine ernsthafte Bedrohung für die Gesundheit von Mensch und Tier darstellen.
Antimikrobielle Peptide (AMPs) sind eine Klasse von basischen Polypeptidsubstanzen mit antimikrobieller Aktivität. Sie haben aufgrund ihrer breit gefächerten antimikrobiellen Eigenschaften und ihrer Letalität gegenüber bestimmten medikamentenresistenten Krankheitserregern Aufmerksamkeit erregt. Die vielfältigen Strukturen nicht-natürlicher Aminosäuren können die Struktur und Funktion von AMPs, wie etwa Hydrophobie, Ladungsdichte und Aktivität, erheblich verändern, wenn natürliche Aminosäuren in antimikrobiellen Peptiden ersetzt werden. Kangs Forschungsgruppe verbesserte nicht nur die antimikrobielle Aktivität gegen penicillinresistente Bakterien erheblich, indem sie Lysin durch Ornithin im Cbf-14-Peptid ersetzte, sondern reduzierte auch dessen Zytotoxizität gegenüber Säugetierzellen. Erwähnenswert ist, dass nicht-natürliche Aminosäuren auch ihre antimikrobielle Wirksamkeit, Zellselektivität und Peptidstabilität verbessern können, indem sie die C- oder N-Termini antimikrobieller Peptide modifizieren. Beispielsweise verbesserte die N-Acetylierungsmodifizierung die antimikrobielle Wirksamkeit und Stabilität von W-MreB erheblich.
Nicht-natürliche Aminosäuren haben nicht nur ein breites Anwendungsspektrum im Bereich der Biomedizin, sondern weisen auch hervorragende organische katalytische Eigenschaften auf. Sie wirken als organische Katalysatoren, die im Vergleich zu anderen katalytischen Methoden im Allgemeinen ungiftig und stabil sind, unempfindlich gegenüber Feuchtigkeit und Luft sind und eine gute Toleranz gegenüber vielen funktionellen Gruppen aufweisen.
Im Bereich der asymmetrischen Synthese können α-unnatürliche Aminosäuren Metallkatalysatoren wirksam ersetzen, um effiziente asymmetrische Synthesereaktionen zu erreichen.
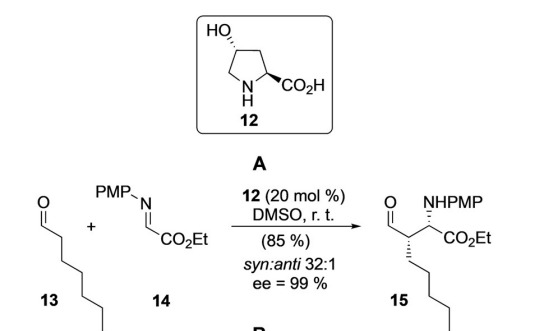
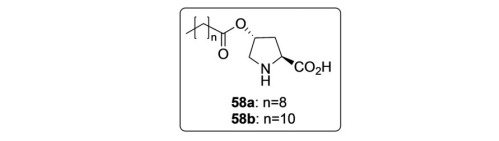
Das Barbas-Team verwendete (2S,4R)-4-Hydroxyprolin als Katalysator, um die Mannich-Reaktion zwischen geradkettigen Fettaldehyden und Iminen erfolgreich zu katalysieren und Mannich-Basen mit hervorragender Ausbeute und Stereoselektivität zu erhalten.
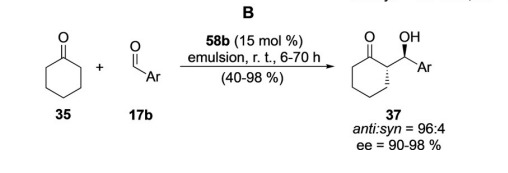
Darüber hinaus ist der Trans-4-Hydroxyprolinester amphiphil und ein Tensid. Zhongs Team nutzte diese Eigenschaft, um die asymmetrische Kondensationsreaktion von Cyclohexanon und aromatischen Aldehyden in einem Emulsionssystem zu katalysieren. Diese Strategie weist nicht nur eine hohe Stereoselektivität auf, sondern erzielt auch gute Reaktionsausbeuten und stellt damit ein neues und leistungsstarkes Werkzeug für die asymmetrische Synthese dar.
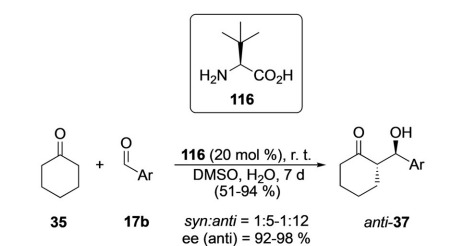
Eine andere Klasse nichtnatürlicher Aminosäuren, L-tert-Leucin und seine Derivate, weisen ebenfalls die Fähigkeit auf, asymmetrische Synthesen zu katalysieren, indem sie die asymmetrische Kondensationsreaktion von Cyclohexanon und aromatischen Aldehyden effektiv mit guter Ausbeute und Stereoselektivität katalysieren.
Unnatürliche Aminosäuren werden häufig verwendet und sind Verbindungen mit hohem Wert und breiten Perspektiven in vielen Bereichen. Obwohl ihr Syntheseprozess ziemlich anspruchsvoll ist, werden mit dem kontinuierlichen Fortschritt von Wissenschaft und Technologie in Zukunft sicherlich effiziente und umweltfreundliche Synthesemethoden entwickelt, wodurch die kontinuierliche Entwicklung des Bereichs der unnatürlichen Aminosäuren gefördert wird.
Haofan Bio ist seit vielen Jahren intensiv in die Forschung und Entwicklung unnatürlicher Aminosäuren involviert und verfügt derzeit über Hunderte von Produkten mit unnatürlichen Aminosäuren. Die folgende Tabelle zeigt einige der Produkte mit unnatürlichen Aminosäuren. Kunden mit Bedarf können uns gerne anrufen, um Anfragen zu stellen.
Referenzen:
[1] Zhao Mei, Liu Xinyuan, Qi Xianghui, et al. Forschungsfortschritt bei der Proteinsynthese basierend auf unnatürlichen Aminosäuren[J]. Food and Fermentation Industries. 2024, 8.
[2] Li Haining, Zhang Hongbing, Jia Zhenhua, et al. Anwendung und Biosynthesestrategie unnatürlicher Aminosäuren[J]. Biotechnology Bulletin. 2023, 39, 43-55.
[3] Narancic, T.; Almahboub, SA; O'Connor, KE Unnatürliche Aminosäuren: Produktion und biotechnologisches Potenzial[J]. World J Microbiol Biotechnol. 2019, 35, 67.
[4] Wang, XH; Yang, XM; Wang, QE; Meng, DM Unnatürliche Aminosäuren: vielversprechende Implikationen für die Entwicklung neuer antimikrobieller Peptide[J]. Critical Reviews in Microbiology. 2023, 49, 231-255.
[5] Agirre, M.; Arrieta, A.; Arrastia, I.; et al. Aus unnatürlichen α-Aminosäuren gewonnene Organokatalysatoren: Umfang und Anwendungen[J]. Chem. Asian J. 2019, 14, 44-66.
[6] Zhong, L.; Gao, Q.; Li, C.; et al. Direkte katalytische asymmetrische Aldolreaktionen an chiralen Katalysatoren, die in der Grenzfläche von Emulsionströpfchen angeordnet sind[J]. J. Catal. 2007, 250,360-364.