I. Hintergrund und Einleitung:
Angesichts der rasanten Entwicklung von Peptidwirkstoffen und anderen Technologien stehen traditionelle Amidsynthesesysteme weiterhin vor zentralen technischen Herausforderungen, wie der Schwierigkeit, Nebenreaktionen zu kontrollieren und die chirale Reinheit zu erhalten. Daher ist die Entwicklung neuer Strategien für eine effiziente und hochselektive Amidsynthese von großer Bedeutung und hohem Anwendungswert.
II. β-Acyloxyalkenylamide (AAAs): Von „Hochtemperatur"-Zwischenprodukten zu „populären" Reagenzien
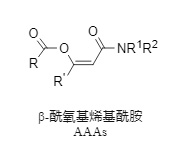
β-Acyloxyalkenylamide (Abbildung 1) sind eine Klasse von Vinylesterverbindungen mit hoher Acylierungsreaktivität. Seit ihrer Entdeckung konnten sie jedoch nur durch ein aufwendiges und komplexes fünfstufiges Syntheseverfahren gewonnen werden. Darüber hinaus ist das wichtige Alkin-Zwischenprodukt wenig stabil, erfordert eine Behandlung bei -50 bis -20 °C und ist schwer zu lagern, was ihre großtechnische Herstellung und Anwendung stark einschränkt.
Abbildung 1
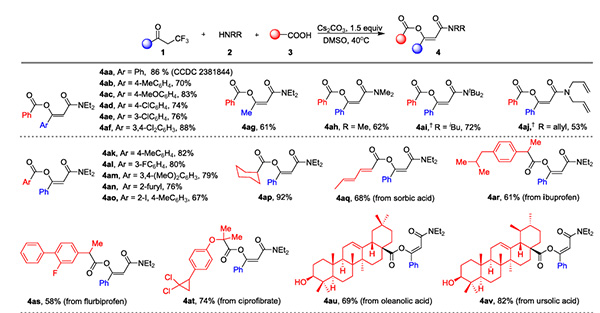
Als Antwort auf dieses langjährige Problem erzielte das Team von Professor Wan Jieping kürzlich einen bedeutenden Durchbruch und entwickelte eine einfache und schonende Methode zur Synthese von β-Acyloxyolefinamiden. Ausgehend von α-Trifluormethylketon, sekundären Aminen und Carbonsäuren als Ausgangsmaterialien und unter Verwendung von Cs₂CO₃ als Katalysator wurde ein kontinuierlicher Defluorierungsprozess eingesetzt, um effizient β-Acyloxyolefinamide mit vielfältigen Strukturen herzustellen (Abbildung 2). Diese Methode ist breit anwendbar und ermöglicht die erfolgreiche Umsetzung von gewöhnlichen Carbonsäuren, geschützten Aminosäuren und bioaktiven Molekülen.
Abbildung 2
III. Anwendungen: Der vielseitige Applikator für β-Acyloxyolefinamide
1. Amide und Peptide
(1) Amidsynthese:
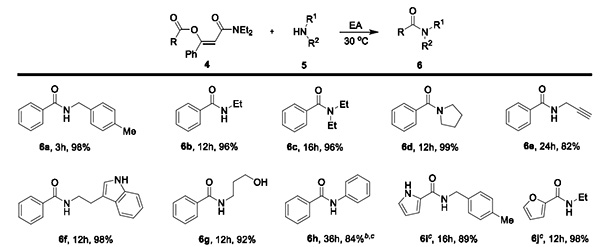
Die mit der neuen Methode synthetisierten β-Acyloxyolefinamide weisen deutliche Vorteile bei der Amidherstellung auf. Unter milden Reaktionsbedingungen (Ethylacetat, 30 °C) lassen sich aliphatische Amine (primäre und sekundäre Amine) sowie aromatische Amine in hohen Ausbeuten der entsprechenden Amide erhalten (Abbildung 3). Zudem zeigt sich eine gute Kompatibilität der β-Acyloxyolefinamide mit unterschiedlichen Strukturen.
Abbildung 3
(2) Peptidsynthese
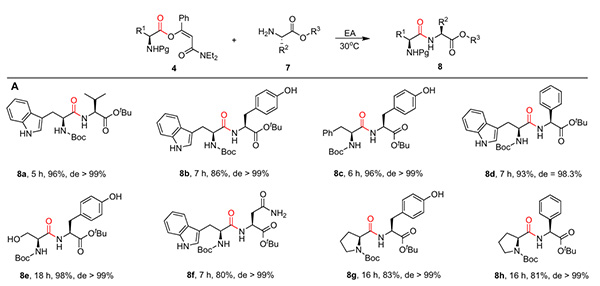
Darüber hinaus untersuchte das Team die Anwendung von β-Acyloxyolefinamiden in der Dipeptidsynthese (Abbildung 4). Ausgehend von Aminosäurederivaten als Ausgangsmaterialien lieferten Amidierungsreaktionen mit verschiedenen Aminosäuren nicht nur das Zieldipeptid in exzellenten Ausbeuten, sondern zeigten auch nahezu keine Racemisierung, was den einzigartigen Vorteil der chiralen Erhaltung unterstreicht.
Abbildung 4
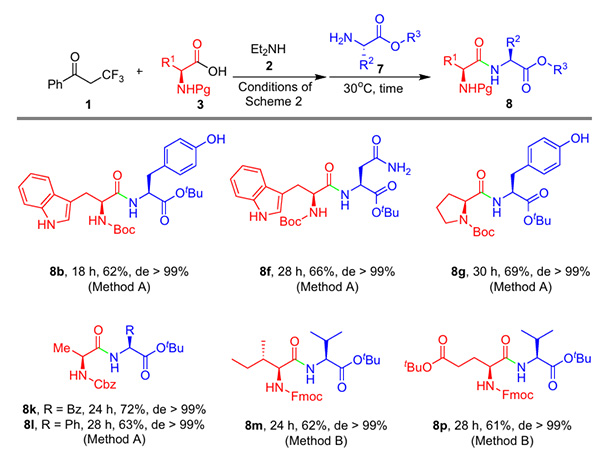
Wie die Ergebnisse zeigen, entwickelte das Team zur weiteren Erforschung der Anwendung von β-Acyloxyalkenylamiden in der Peptidsynthese eine Eintopf-Zweistufen-Synthesestrategie (Abbildung 5): Ausgehend von α-Trifluormethylacetophenon, Diethylamin und N-geschützten Aminosäuren wurden zunächst β-Acyloxyalkenylamide in einer Dreikomponentenreaktion hergestellt. Ohne vorherige Trennung und Reinigung wurden diese direkt mit Aminosäureestern gekuppelt, um die entsprechenden Dipeptide in mäßigen bis guten Ausbeuten zu erhalten. Dabei blieb die chirale Integrität während des gesamten Prozesses erhalten, was die Syntheseeffizienz deutlich verbesserte.
Abbildung 5
(3) Racemisierungsexperiment
Um die Racemisierungshemmung von β-Acyloxyalkenylamiden in der Peptidsynthese objektiv zu bewerten, verglich das Team die Reaktion von β-Acyloxyalkenylamiden mit DCC und HBTU unter gleichen Bedingungen. Die Ergebnisse zeigten, dass die Reaktion mit DCC eine signifikante Racemisierung aufwies (dr = 97,6), während die Racemisierungshemmung bei β-Acyloxyalkenylamiden mit der von HBTU vergleichbar war (dr > 99).
2. Estersynthese
Diese Strategie lässt sich auch auf die Synthese von Estern ausweiten, jedoch sind die Reaktionsbedingungen im Vergleich zu Aminen relativ harsch und erfordern eine Durchführung der Reaktion bei 100 °C unter Zugabe von DBU. Unter diesen Bedingungen betrug die Esterausbeute der Reaktion mit Benzylalkohol 94 % und die der Reaktion mit Phenol 64 % (Abbildung 6).
Abbildung 6
IV. Gesamtschlussfolgerung: β-Acyloxyalkenylamide – Ein neues Synthesewerkzeug
Zusammenfassend lässt sich sagen, dass die von Wan Jiepings Team entwickelte neue Methode zur Synthese von β-Acyloxyalkenylamiden ein breites Substratspektrum abdeckt, ein langjähriges Syntheseproblem auf diesem Gebiet löst und den Wandel von „schwer zugänglich" zu „leicht verfügbar" vollzieht. Diese Verbindungen zeigen hervorragende Ergebnisse in der Amid- und Peptidsynthese und bieten Vorteile wie milde Reaktionsbedingungen, einfache Handhabung und gute Stereoselektivität ohne den Bedarf an zusätzlichen Additiven. Insbesondere die entwickelte Eintopf-Zweistufen-Synthesestrategie verbessert die Stufenökonomie und eröffnet neue Syntheseansätze für die Peptid- und Wirkstoffsynthese.
Unternehmensvorstellung:
Suzhou Highfine Biotech Co., Ltd. (Börsenkürzel: 301393.SZ), gegründet 2003 und ansässig in der Suzhou High-Tech-Zone, ist ein nationales Hightech-Unternehmen, das Spezialrohstoffe für die pharmazeutische Forschung und Entwicklung sowie die Produktion weltweit anbietet. Die Produkte werden hauptsächlich in der Peptid-, Nukleotid- und pharmazeutischen Synthese eingesetzt und umfassen ein breites Spektrum, darunter Kondensationsmittel für die spezielle Amidbindungsknüpfung, Schutzmittel, Vernetzungsmittel, Proteinvernetzungsmittel für Antikörper-Wirkstoff-Konjugate, molekulare Bausteine, Liposomen und Phosphorreagenzien. Aktuell entwickelt und produziert das Unternehmen über 1500 Produkte.
Nach mehr als zwei Jahrzehnten kontinuierlicher Anstrengungen und stetiger Weiterentwicklung hat Highfine Biotech seine Expertise im Bereich globaler Peptidsynthese-Reagenzien kontinuierlich ausgebaut und sich zu einem führenden Unternehmen mit einem umfassenden Angebot an kundenspezifischen Produkten und bedeutenden Vorteilen in der Großproduktion entwickelt, das in der Lage ist, die spezifischen Bedürfnisse verschiedenster Kunden zu erfüllen. Wir laden interessierte Kunden herzlich ein, sich für weitere Informationen und zur Besprechung von Kooperationsmöglichkeiten mit uns in Verbindung zu setzen.
Referenzen:
[1] Cao, SF.; Guo, HJ; Wan, JP, et al. β-Acyloxyl-Alkenylamid-Synthese durch mehrfache Defluorierung: α-Trifluormethylketon-Amin als synergistisches Peptidkupplungsreagenz [J]. Sci. Adv., 2025, 11.
[2] Cao, Sufang. Einstufige Synthese von β-Acyloxyl-Alkenylamid basierend auf CF-Bindungsaktivierung und ihre Anwendung in der Synthese von Amiden und Peptiden [D]. Jiangxi Normal University, 2025.