1. Molekulare Eigenschaften von Boc-Oxyma:
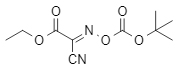
Boc-Oxyma (Strukturformel siehe Abbildung 1) vereint die Aminoschutzfähigkeit von Boc-Anhydrid mit der Kupplungsaktivität von Oxyma und erfüllt so die Doppelfunktion eines Schutz- und Kupplungsreagenz. Es bietet die Vorteile hoher Stabilität, geringer Toxizität und einfacher Handhabung und bietet damit eine neue Option für die grüne chemische Synthese.
Abbildung 1 Boc-Oxyma-Struktur
2. Dualer Funktionsmechanismus von Boc-Oxyma:
1. Amino-Schutzreagenz: Überwindung traditioneller Beschränkungen
Die konventionelle Methode zur Einführung von tert-Butyloxycarbonyl (Boc)-Schutzgruppen beruht hauptsächlich auf Di-tert-butyldicarbonat (Boc-Anhydrid) und halogenierten Formiatreagenzien. Diese Reagenzien sind jedoch mit Problemen wie geringer Stabilität und schwieriger Reinigung behaftet. Boc-Oxyma hingegen weist dank seiner hervorragenden Stabilität, Umweltverträglichkeit und breiten Substratanwendbarkeit erhebliche technische Vorteile auf. Insbesondere:
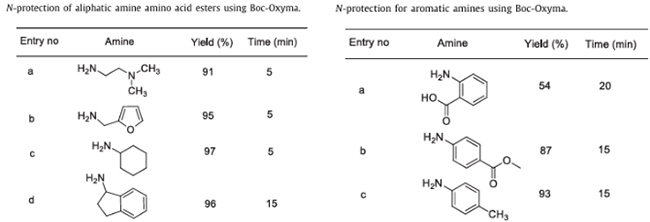
(1) Breite Substratanwendbarkeit: Wie in Abbildung 2 dargestellt, kann ein wirksamer Schutz für aliphatische Amine, aromatische Amine und gehinderte Amine (sekundäre Amine) erreicht werden;
(2) Es liegt eine Regulierung durch den elektronischen Effekt vor: Bei aromatischen Aminen führt gemäß dem Gesetz des elektronischen Effekts für aromatische Verbindungen das Vorhandensein von elektronenspendenden Gruppen an den ortho-para-Positionen aromatischer Amine zu einer höheren Ausbeute (über 90 %), während elektronenziehende Gruppen zu einer geringeren Reaktionsausbeute führen;
(3) Grüne Reagenzien: Bei der Reaktion entsteht nur das wenig toxische Nebenprodukt Oxyma, das recycelt und wiederverwendet werden kann. Dadurch wird die Abfallproduktion effektiv reduziert und die Entwicklungsanforderungen der grünen synthetischen Chemie erfüllt.
Abbildung 2 Experiment zum Schutz der Aminogruppe mit Boc-Oxyma
2. Kupplungsreagenz: Aufbau mehrerer Produkte
Boc-Anhydrid ist ebenfalls ein Kupplungsreagenz, das mit Carbonsäure ein gemischtes Anhydrid-Zwischenprodukt bildet und dann eine Kupplungsreaktion mit Amino-/Hydroxygruppen durchläuft. Bei diesem Prozess entstehen jedoch leicht Nebenprodukte. Boc-Oxyma ermöglicht eine schonende und effiziente Kupplung über die Aktivesterroute. Die technischen Vorteile sind im Einzelnen wie folgt:
(1) Aufbau mehrerer funktioneller Strukturen:
① Verwendung von Carbonsäure als Substrat:
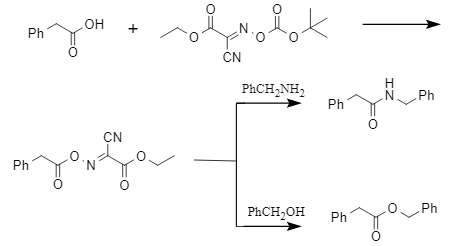
Die durch Boc-Oxyma geförderte Carbonsäure-Kupplungsreaktion ermöglicht den effizienten Aufbau wichtiger funktioneller Strukturen wie Esterbindungen, Thioesterbindungen und Amidbindungen. Es zeigt eine universelle Aktivierungsfähigkeit für Fett-, Aromaten-, langkettige und Aminosäuren. Am Beispiel der Modellreaktion mit Phenylessigsäure kann die Kupplungseffizienz mit Benzylalkohol und Benzylamin über 90 % erreichen. Der Wirkungsmechanismus von Boc-Oxyma besteht in der Bildung eines aktiven Oxyanhydridesters einer Carbonsäure, gefolgt von einem nukleophilen Angriff, um den Bindungsprozess abzuschließen, wie in Abbildung 3 dargestellt:
Abbildung 3 Wirkungsmechanismus von Boc-Oxyma
2. Verwendung von Hydroxamsäure als Substrat:
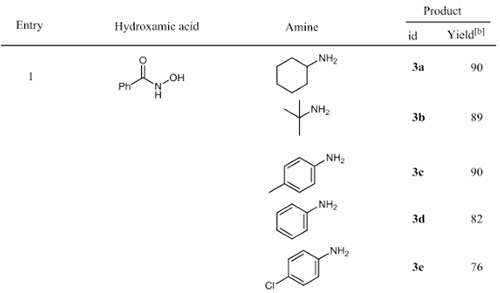
Unter Beteiligung von Boc-Oxyma durchläuft Hydroxamsäure eine Lossen-Umlagerung zum entsprechenden Isocyanat. Unter Einwirkung von Amin-Nukleophilen können die entsprechenden Harnstoffderivate durch eine Reaktion bei Raumtemperatur erhalten werden (siehe Abbildung 4). Im Vergleich zur traditionellen Hofmann-Reaktion, die hochvalentes Iod benötigt, und der Curtius-Reaktion mit Azid ist diese Reaktion sicherer und schonender.
Darüber hinaus kann im System mit koexistierenden Hydroxy- und Aminogruppen selektiv mit Aminogruppen bei Raumtemperatur reagiert werden, um Harnstoffderivate zu bilden. Während bei der Reaktion mit Alkoholen/Thiolen DMAP-Katalyse und Erhitzen erforderlich sind, um die entsprechenden Carbamat- und Thiocarbamatverbindungen zu erhalten.
Abbildung 4 Boc-Oxyma-vermittelte Hydroxamsäure-Kupplungsreaktion
(2) Stereoselektive Regulierung: Am Beispiel des Tripeptidsyntheseexperiments zeigte
Boc-Oxyma nicht nur eine effiziente Kopplungsfähigkeit, sondern auch eine hervorragende Stereostrukturkontrolle. Im Vergleichsexperiment zur Racemisierung der Tripeptidsynthese zeigte Boc-Oxyma hervorragende Ergebnisse, ohne dass Racemisierung beobachtet wurde. Einzelheiten siehe Tabelle 1 unten.
Tabelle 1 Racemisierungsvergleichstest
(3) Umweltfreundliches und nachhaltiges Reaktionssystem
Das Boc-Oxyma-System weist herausragende Leistungen in Bezug auf Atomökonomie und Umweltschutz auf:
1. Die meisten Kupplungsreaktionen, an denen es beteiligt ist, werden bei Raumtemperatur und geringem Energieverbrauch durchgeführt;
2. Das entstehende Nebenprodukt Oxyma kann mit hoher Auslastung und geringen Kosten recycelt und wiederverwendet werden;
3. Die verbleibenden Nebenprodukte (tert-Butylalkohol, Kohlendioxid) sind wenig toxisch und der Ausstoß dreier Abfallprodukte ist relativ gering.
Zusammenfassend lässt sich sagen, dass Boc-Oxyma die Wirtschaftlichkeit der Synthese durch die Eigenschaft „eine Dosis für mehrere Anwendungen" deutlich verbessert, eine neue Syntheseidee für die Peptidsynthese und deren industrielle Produktion liefert und bedeutenden Anwendungswert und -potenzial besitzt.
Nach 22 Jahren unermüdlicher Anstrengungen und Aufbau hat Highfine Bio seine Wurzeln im Bereich der globalen Peptidsynthesereagenzien weiter vertieft und sich nun zu einem führenden Unternehmen mit umfassender Abdeckung maßgeschneiderter Produkte und erheblichen Vorteilen bei der Produktion im großen Maßstab entwickelt. Das Unternehmen ist nun in der Lage, Boc-Oxyma-Produkte in unterschiedlichen Spezifikationen bereitzustellen, um die speziellen Anforderungen verschiedener Kunden zu erfüllen. Kunden, die an diesem Produkt interessiert sind, laden wir herzlich ein, sich mit uns in Verbindung zu setzen, um mehr über die Produktdetails zu erfahren und Kooperationsmöglichkeiten auszuloten.
Referenzen:
[1] Robert, AR; Kumar, GR; Jonnalagadda, SB, et al.. Eine neuartige Verwendung von Boc-Oxyma als Reagenz für die tert-Butoxycarbonylierung von Aminen und Aminosäureestern[J]. Chemical Data Collections, 2020, 30.
[2] Thalluri, K.; Nadimpally, KC; Mandal, B.; et al. Ethyl-2-(tert-Butoxycarbonyloxyimino)-2-cyanoacetat (Boc-Oxyma) als Kupplungsreagenz für racemisierungsfreie Esterifizierung, Thioesterifizierung, Amidierung und Peptidsynthese[J]. Adv. Synth. [3] Manne, SR; Thalluri, K.; Mandal
, B.; et al. Ethyl-2-(tert-Butoxycarbonyloxyimino)-2-cyanacetat (Boc-Oxyma): Ein effizientes Reagenz für die racemisierungsfreie Synthese von Harnstoffen, Carbamaten und Thiocarbamaten mittels Lossen-Umlagerung[J]. Adv. Synth. Catal., 2017, 359, 168–176.