Dieser Artikel stellt kurz die Phthaloyl-Reihe der Amino-Schutzgruppen vor.
1. Einleitung
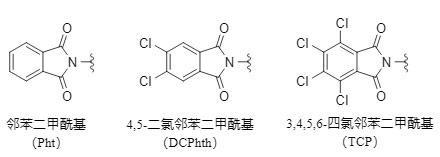
Phthaloyl und seine Derivate sind eine Art häufig verwendeter Amino-Schutzgruppen (siehe Struktur in der Abbildung unten, im Folgenden zusammenfassend als Phthaloyl bezeichnet, und spezifische Schutzgruppen werden durch ihre Abkürzungen dargestellt), die häufig bei der Synthese komplexer organischer Moleküle, insbesondere Peptiden und Zuckern, verwendet werden.
Abbildung 1 Gängige Phthalsäure-Schutzgruppen
Phthaloyl wird üblicherweise zum Schutz primärer Amine verwendet. Es bleibt unter konventionellen sauren Bedingungen, katalytischer Hydrogenolyse und NH3(l)/Na-Reduktionssystemen stabil. Im Vergleich zu anderen Acylschutzgruppen ermöglicht Phthaloyl eine vollständige Substitution von Aminogruppen und verhindert so effektiv die Racemisierung in der Peptidsynthese. Unter alkalischen Bedingungen und in Gegenwart starker Nukleophile ist es jedoch instabil, weshalb häufig Hydrazinhydrat zur Entschützung eingesetzt wird.
2. Einführungsmethode
1. Phthalsäureanhydrid-Methode
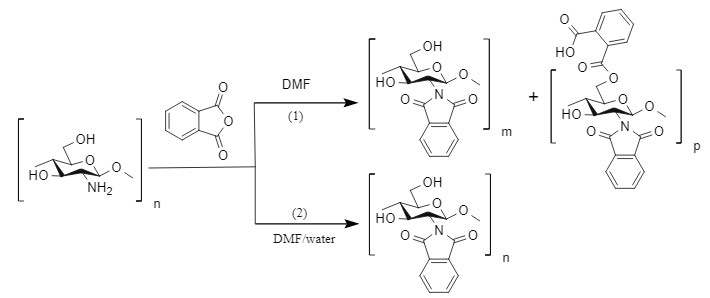
Kurita et al. verwendeten Phthalsäureanhydrid in einer DMF-Lösung mit 5 % Wasser bei 120 °C, um die Pht-Schutzgruppe beim Schutz der Aminogruppe von Chitosan einzuführen, mit einer Ausbeute von >80 %. Unter dieser Bedingung kann die Aminogruppe selektiv geschützt werden, während die Hydroxygruppe unberührt bleibt (Methode 2). Kurita et al. fanden außerdem heraus, dass bei Durchführung der Reaktion in reinem DMF ein Nebenprodukt entsteht, in dem sowohl die Aminogruppe als auch die Hydroxygruppe geschützt sind (Methode 1).
Diese Methode muss üblicherweise bei höheren Temperaturen durchgeführt werden. Enthält das Molekül mehrere Aminogruppen (sekundäre und primäre Amine nebeneinander), treten wahrscheinlich Nebenreaktionen mit sekundären Aminen auf. Diese Methode ist jedoch relativ einfach nachzubearbeiten und eignet sich für die industrielle Produktion.
2. Monoethylphthalat-Methode
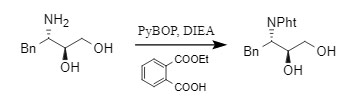
Aguilar et al. verwendeten Monoethylphthalat in Gegenwart einer Base (z. B. DIEA) und des Kondensationsreagenzes PyBOP, um die Amidreaktion zu fördern und so eine Pht-Schutzgruppe einzuführen.
Diese Methode ist relativ umständlich und zeitaufwendig. Sie ist zudem nicht für die Koexistenz mehrerer Aminogruppen geeignet.
3. N-Ethoxycarbonylphthalimid-Methode
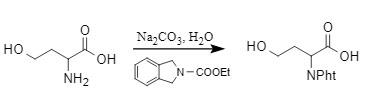
Jonghe et al. verwendeten N-Ethoxycarbonylphthalimid, um die Pht-Schutzgruppe unter alkalischen Bedingungen beim Schutz der Aminogruppe einzuführen
.
Diese Methode ist schonend, kostengünstig und kann primäre Amine in Gegenwart sekundärer Amine selektiv schützen. Sie ist derzeit eine gängige Einführungsmethode.
Khalifa et al. entwickelten eine Methode zur effizienten Einführung einer Pht-Schutzgruppe durch N-Benzolsulfonylphthalimid (hergestellt durch die Reaktion von Phthalimid und Benzolsulfonylchlorid). Diese Methode ermöglicht die Einführung von Pht unter Acetonitril-Rückflussbedingungen mit hoher Ausbeute und ohne zusätzliche Base. Sie ist auf eine Vielzahl aromatischer und aliphatischer Amine anwendbar.
3. Entfernungsmethode
Es ist wichtig, eine geeignete Entfernungsmethode zu wählen, die nicht nur eine hohe Entfernungseffizienz aufweist, sondern auch gewährleistet, dass andere Schutzgruppen nicht beeinträchtigt werden.
1. Hydrazinolysemethode: Normalerweise wird die Pht-Schutzgruppe durch Hydrazinhydrolyse entfernt. Im Allgemeinen kann sie durch Rückflusskochen in einer alkoholischen Hydrazinhydratlösung vollständig entfernt werden. Unter dieser Bedingung werden Cbz, Boc, Ts, Trt und andere Schutzgruppen nicht beeinträchtigt.
2. NaBH4/i-PrOH/AcOH-Methode: Diese Methode ist eine Ergänzung zur Hydrazinhydrolysemethode. Wenn die Hydrazinhydrolysewirkung nicht gut ist, kann Pht unter diesen Bedingungen gut entfernt werden.
3. Ethylendiaminmethode: Die Tetrachlorphthaloylgruppe (TCP) in dieser Reihe wird in Gegenwart von Ethylendiamin selektiv entfernt, während die Estergruppe und Pht nicht beeinträchtigt werden.
4. Synthesestrategie
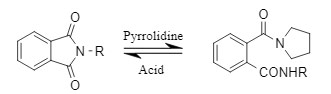
Die Pht-Schutzgruppe kann vorübergehend deaktiviert werden, um den normalen Ablauf anderer Reaktionen zu gewährleisten. Anschließend kann die Strategie der „Wiederbelebung" in bestimmten Fällen angewendet werden. Aufgrund der geringen Stabilität von Pht in Gegenwart alkalischer und nukleophiler Reagenzien kann es mit Tetrahydropyrrol umgesetzt werden, um ein stabileres Derivat zu erhalten. Nach Abschluss anderer Reaktionen kann es unter sauren Bedingungen zu einer Pht-Gruppe regeneriert werden und weiterhin an nachfolgenden Reaktionen teilnehmen.
In diesem Artikel werden die Methoden zur Einführung und Entfernung der Aminoschutzgruppe Phthaloyl und ihre erweiterte Anwendung in Synthesestrategien beschrieben. Er soll Fachleuten in ähnlichen Bereichen als Referenz und Anregung dienen.
Referenzen:
[1] Guo Yanhao, Hao Qinghui, Hao Siyuan, et al. Schutz und Entschützung von Aminogruppen in chemischen Produkten[J]. Coal and Chemical Industry, 2022, 45, 106-112.
[2] Kurita, K.; lkeda, H.; Harata, M.; et al. Chemoselektiver Schutz der Aminogruppen von Chitosan durch kontrollierte Phthaloylierung: Einfache Herstellung einer für chemische Modifikationen nützlichen Vorstufe[J]. Biomacromolecules, 2002, 3.
[3] Aguilar, N.; Moyano, A.; Pericàs, MA; Riera, A. Eine allgemeine, katalytische und enantioselektive Synthese von (S)-γ-[(S)-1-Aminoalkyl]-γ-lactonen[J]. J. Org. Chem. 1998, 63, 3560-3567.
[4] Jonghe, SD; Lamote, I.; Herdewijn. P; et, al. Synthese von Homoceramiden, neuartigen Ceramid-Analoga und deren fehlender Effekt auf das Wachstum hippocampaler Neuronen[J]. J. Org. Chem. 2002, 67, 988-996.
[5] Khalifa, A.; Giles, M.; Ali, HI; Mohamady, S. Metall- und katalysatorfreie Synthese von 2-substituierten Phthalimiden unter Verwendung von 2-(Arensulfonyl)Phthalimid als Schlüsselreagenzien[J]. Eur. J. Org. Chem. 2023, 26.
[6] Debenham, JS; Fraser-Reid, B. Tetrachlorophthaloyl als vielseitige Amin-Schutzgruppe[J]. J.Org.Chem.1996,61,432-433.
[7] Astleford, B.; Weigel, LO „Anwendungsbereich der Phthalimidochemie I. Erweiterung des Nutzens durch Umwandlung in die OPCB-Schutzgruppe."[J]. Tetrahedron Lett., 1991, 32, 3301-3304.